题目内容
【题目】新合成的一种烃,其碳架呈三棱柱体(如图所示),称为棱晶烷。
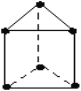
(1)写出该烃的分子式为_____________。
(2)该烃的一氯取代物有_________种,二氯取代物有______种。
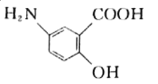
(3)该烃的同分异构体有多种,其中1种不能使酸性高锰酸钾溶液或Br2-CCl4溶液褪色,但在一定条件下能跟溴(或H2)发生取代(或加成)反应,写出在浓硫酸作用下,这种同分异构体与浓硝酸反应的化学方程式______________________________________________。
(4)有同学认为棱晶烷与立方烷( 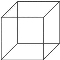 )互为同系物,判断这种观点是否正确并说明理由_______________________________。
)互为同系物,判断这种观点是否正确并说明理由_______________________________。
【答案】C6H6 1 3 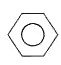 +HNO3
+HNO3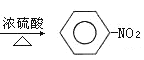 +H2O 不是,立方烷的分子式为C8H8,和棱晶烷在组成相差C2H2,不符合同系物的定义
+H2O 不是,立方烷的分子式为C8H8,和棱晶烷在组成相差C2H2,不符合同系物的定义
【解析】
(1)根据键线式来书写分子式;(2)根据对称性原则来判断烃中的等效氢原子,进而判断一氯代物、二氯代物的种数;(3)根据限制条件分析同分异构体的结构,并根据其性质书写相关反应方程式;(4)根据图示的有机物结构及同系物的概念分析解答。
(1)根据有机物键线式的特点,可知该有机物分子式为C6H6,故答案为:C6H6;
(2)该有机物中的6个氢原子完全等效,所以其一氯代物只有一种;将三棱柱体的一个顶点固定,该碳上的氢原子被氯原子取代,则与该碳共面的另一个点、竖棱上的共线点以及以及对角线上的点上的氢原子被氯原子代替时均不同,所以该烃的二氯取代物有3种,故答案为:1;3;
(3)不能使酸性高锰酸钾溶液或溴水溶液褪色,但在一定条件下能跟溴发生取代反应、与H2发生加成反应,符合分子式C6H6的烃是苯,苯和浓硝酸在浓硫酸作用下反应生成硝基苯和水,反应方程式为:  +HNO3
+HNO3![]()
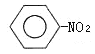 +H2O,故答案为:
+H2O,故答案为: +HNO3
+HNO3![]()
 +H2O;
+H2O;
(4)根据棱晶烷与立方烷结构分析,它们不是同系物,原因是,立方烷的分子式为C8H8,和棱晶烷在组成相差C2H2,不符合同系物的定义,故答案为:不是,立方烷的分子式为C8H8,和棱晶烷在组成相差C2H2,不符合同系物的定义。

 新思维寒假作业系列答案
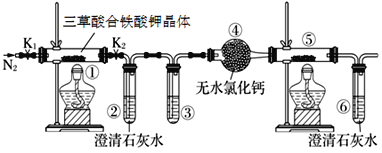
新思维寒假作业系列答案【题目】下表是某同学探究Na2SO3溶液和铬(VI)盐溶液反应规律的实验记录,已知:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黄色)+ 2H+
2CrO42-(黄色)+ 2H+
序号 | a | b | 现象 | |
| 1 | 2 mL 0.05 mol·L1 K2Cr2O7溶液(pH = 2) | 3滴饱和Na2SO3溶液(pH = 9) | 溶液变绿色(含Cr3+) |
2 | 2 mL 0.1 mol·L1 K2CrO4溶液(pH = 8) | 3滴饱和Na2SO3溶液 | 溶液没有明显变化 | |
3 | 2 mL饱和Na2SO3溶液 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变黄色 | |
4 | 2 mL蒸馏水 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液变成浅橙色 |
下列说法不正确的是
A. 实验1中的绿色溶液中含有SO42-
B. 实验1、2的a溶液中所含的离子种类相同
C. 向实验3溶液中继续滴加过量硫酸可使溶液变为浅橙色
D. 实验4的目的是排除稀释对溶液颜色变化造成的影响
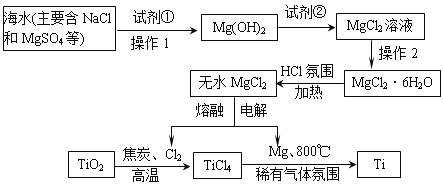
【题目】目前世界上60%的镁是从海水中提取的,从海水中提取的MgCl2制得Mg和Cl2,进一步联合用金红石(主要成分TiO2)冶炼金属钛,工业上其主要的生产流程如下:
|
回答下列问题:
(1)加入过量试剂①后,能够分离得到Mg(OH)2沉淀的方法操作1用到的玻璃仪器有________________________________________;试剂②可以选用______。
(2)要得到MgCl2·6H2O的操作2名称是___________________________________。
(3)工业上冶炼金属钛的上述生产流程,其第1步是在高温下向金红石(主要成分TiO2)与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体,写出这步反应的化学方程式:____________________________。
(4) 工业上冶炼金属钛的上述生产流程,其第2步是在稀有气体氛围和加热的条件下,用镁与TiCl4反应得到钛,写出这步反应的化学方程式____________________,该反应时稀有气体氛围的作用是_____________________________________,该反应的金属冶炼方法属于是____________________。