题目内容
12.碘在不同状态下(固态或气态)与氮气反应的热化学方程式如下所示:①H2(g)+I2(?)?2HI(g)△H=+9.48kJ•mol-1
②H2(g)+I2(?)?2HI(g)△H=-26.48kJ•mol-1
下列刘断正确的是( )
| A. | ①中的为气态.②中的为固态 | |
| B. | ①的反应物总能量比②的反应物总能量低 | |
| C. | ①的产物比反应②的产物热稳定性更好 | |
| D. | 1mol固态碘升华时将吸热17kJ |
分析 根据同种物质气态时具有的能量比固态时高,所以等量时反应放出能量高,已知反应①吸收能量,反应②放出能量,所以反应②中碘的能量高,则反应①中碘为固态,②中的I2为气态,据此分析.
解答 解:A.已知反应①吸收能量,反应②放出能量,所以反应②中碘的能量高,则反应①中碘为固态,②中的I2为气态,故A错误;
B.已知反应①吸收能量,反应②放出能量,所以反应②中碘的能量高,所以①的反应物总能量比②的反应物总能量低,故B正确;
C.反应①②的产物都是气态碘化氢,所以二者热稳定性相同,故C错误;
D.根据盖斯定律,①-②为,即I2(s)?I2(g))△H=+35.96KJ/mol,故D错误.
故选B.
点评 本题考查了反应中的能量变化,注意同种物质气态时能量大于固态,题目难度不大.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
2.工业生产苯乙烯是利用乙苯的脱氢反应: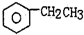 (g)$\stackrel{560℃}{?}$
(g)$\stackrel{560℃}{?}$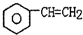 (g)+H2(g)△H<0
(g)+H2(g)△H<0
针对上述反应,在其它条件不变时,下列说法正确的是( )
 (g)$\stackrel{560℃}{?}$
(g)$\stackrel{560℃}{?}$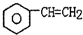 (g)+H2(g)△H<0
(g)+H2(g)△H<0针对上述反应,在其它条件不变时,下列说法正确的是( )
| A. | 加入适当催化剂,可以提高乙苯的转化率 | |
| B. | 在保持体积一定的条件下,充入较多的乙苯,可以提高乙本的转化率 | |
| C. | 在加入乙苯至达到平衡过程中,混合气体的平均相对分子质量不变 | |
| D. | 仅从平衡移动的角度分析,工业生产苯乙稀选择恒压条件优于恒容条件 |
3.短周期主族元素X、Y、Z的原子序数依次增大,在周期表中分处三个不同周期.X与Z同主族,X与Z的原子序数之和为12.下列说法中不正确的是( )
| A. | 离子半径 Z>X | B. | 最外层电子数 Z>Y | ||
| C. | 金属性 Z>X | D. | 原子半径 Z>Y |
20.下列反应不属于氧化还原反应的是( )
| A. | CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 | B. | Cl2+H2O?HCl+HClO | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |


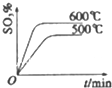

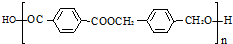 的路线:
的路线: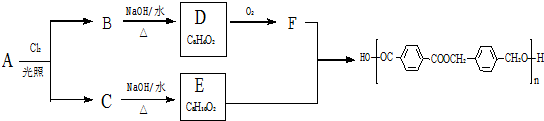
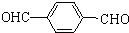 ,由B生成D的反应过程中生成的不稳定中间体的结构简式是
,由B生成D的反应过程中生成的不稳定中间体的结构简式是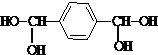 ,该中间体生成D的反应类型为消去反应.
,该中间体生成D的反应类型为消去反应.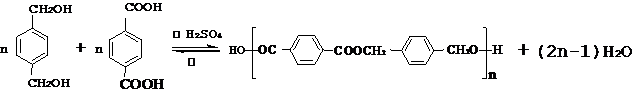 ,反应类型为缩聚反应.与E具有相同官能团的含苯环的同分异构体有(写结构简式)
,反应类型为缩聚反应.与E具有相同官能团的含苯环的同分异构体有(写结构简式)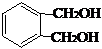 、
、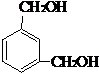 、
、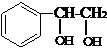 .
.