题目内容
4.以下是某课题组设计的由烃A合成聚酯类高分子材料.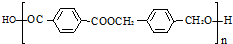 的路线:
的路线: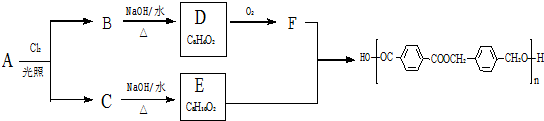
已知同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮.
根据以上信息回答:
(1)A的分子式C8H10,F中官能团的名称是羧基.
(2)化合物D的结构简式是
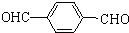 ,由B生成D的反应过程中生成的不稳定中间体的结构简式是
,由B生成D的反应过程中生成的不稳定中间体的结构简式是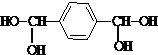 ,该中间体生成D的反应类型为消去反应.
,该中间体生成D的反应类型为消去反应.(3)E与F反应的化学方程式是
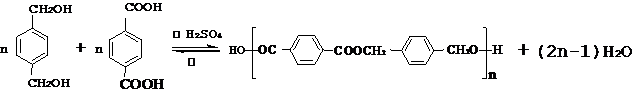 ,反应类型为缩聚反应.与E具有相同官能团的含苯环的同分异构体有(写结构简式)
,反应类型为缩聚反应.与E具有相同官能团的含苯环的同分异构体有(写结构简式)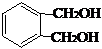 、
、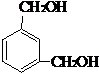 、
、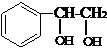 .
.
分析 根据题中各物质转化关系,E和F发生缩聚反应得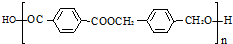 ,且F是由D氧化得到,所以E为
,且F是由D氧化得到,所以E为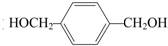 ,F为
,F为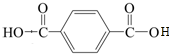 ,所以D为
,所以D为 ,由同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮可知,B为
,由同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮可知,B为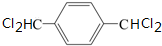 ,C为
,C为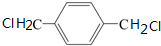 ,所以烃A为
,所以烃A为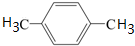 ,据此答题.
,据此答题.
解答 解:根据题中各物质转化关系,E和F发生缩聚反应得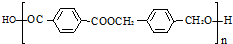 ,且F是由D氧化得到,所以E为
,且F是由D氧化得到,所以E为 ,F为
,F为 ,所以D为
,所以D为 ,由同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮可知,B为
,由同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮可知,B为 ,C为
,C为 ,所以烃A为
,所以烃A为 ,
,
(1)根据上面的分析可知,A为 ,所以A的分子式为C8H10,F为
,所以A的分子式为C8H10,F为 ,所以F中官能团的名称是羧基,
,所以F中官能团的名称是羧基,
故答案为:C8H10;羧基;
(2)根据上面的分析可知,化合物D的结构简式是 ,由B生成D的反应过程是B中的氯原子被羟基取代,所以反应过程中生成的不稳定中间体的结构简式是
,由B生成D的反应过程是B中的氯原子被羟基取代,所以反应过程中生成的不稳定中间体的结构简式是  ,该中间体生成D是两个羟基脱去一分子水形成碳氧双键,所以反应类型为消去反应,
,该中间体生成D是两个羟基脱去一分子水形成碳氧双键,所以反应类型为消去反应,
故答案为: ;
; ;消去反应;
;消去反应;
(3)E与F反应的化学方程式是 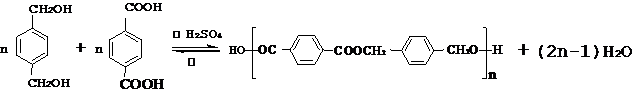 ,反应类型为缩聚反应,E为
,反应类型为缩聚反应,E为 ,与E具有相同官能团的含苯环的同分异构体有
,与E具有相同官能团的含苯环的同分异构体有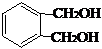 、
、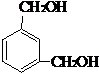 、
、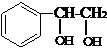 ,
,
故答案为: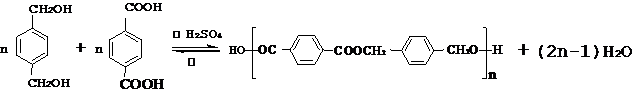 ;缩聚反应;
;缩聚反应;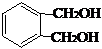 、
、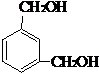 、
、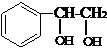 .
.
点评 本题考查有机物推断与合成,是对有机化学基础的综合考查,根据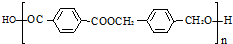 利用反推法确定有机物是解题的关键,需要学生熟练掌握官能团的性质与转化,难度中等.
利用反推法确定有机物是解题的关键,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
相关题目
15.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(l)△H=-483.6 kJ•mol-1,则 2molH2(g)和1molO2(g)所含有的总能量比2mol H2O(l)所含有的总能量少483.6kJ | |
| B. | 己知2C(s)+2O2(g)═2CO2(g)△H12C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 利用盖斯定律可以间接计算通过实验难以测定反应的反应热 |
12.碘在不同状态下(固态或气态)与氮气反应的热化学方程式如下所示:
①H2(g)+I2(?)?2HI(g)△H=+9.48kJ•mol-1
②H2(g)+I2(?)?2HI(g)△H=-26.48kJ•mol-1
下列刘断正确的是( )
①H2(g)+I2(?)?2HI(g)△H=+9.48kJ•mol-1
②H2(g)+I2(?)?2HI(g)△H=-26.48kJ•mol-1
下列刘断正确的是( )
| A. | ①中的为气态.②中的为固态 | |
| B. | ①的反应物总能量比②的反应物总能量低 | |
| C. | ①的产物比反应②的产物热稳定性更好 | |
| D. | 1mol固态碘升华时将吸热17kJ |
19.用惰性电极电解一定量的硫酸铜溶液.实验装置如图甲.电解过程中的实验数据如图乙,横坐标表示电解过程中转移电子的物质的量.纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法不正确的是( )


| A. | 电解过程中,a电极表面先有红色物质析出.后有气泡产生 | |
| B. | b电极上发生氧化反应.共产物为H2O和O2 | |
| C. | 曲线O-P段表示O2的体积变化,p-Q段表示H2的体积变化 | |
| D. | 从开始到Q点.共收集到0.1molH2和0.1molO2 |
9.下列对氧化还原反应的分析中不合理的是( )
| A. | Mg变为MgO时化合价升高,故Mg在该反应中作还原剂 | |
| B. | 在反应2H2S+SO2═3S+2H2O中,氧化产物和还原产物都是S | |
| C. | 凡是置换反应都是氧化还原反应 | |
| D. | 在反应2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑中,H2是还原剂 |
14.常温下在水中加入下列物质,不会破坏水的电离平衡的是( )
| A. | 通入HCl气体 | B. | 加入碳酸钠固体 | C. | 加入蔗糖 | D. | 加入金属钠 |
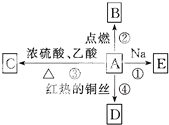 A是化学实验室中最常见的有机物,能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,能进行如图所示的多种反应. CH3COOCH2CH3+H2O;反应④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
CH3COOCH2CH3+H2O;反应④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
 (注明条件).
(注明条件). 、
、
 与1分子CH2=CHCOOCH2
与1分子CH2=CHCOOCH2 在一定条件下可发生类似反应①的反应,生成有机化合物W,W的结构简式为
在一定条件下可发生类似反应①的反应,生成有机化合物W,W的结构简式为 .
.