题目内容
17.下列关于反应2SO2(g)+O2(g)?2SO2(g)△H=-196kJ•mol-1的图象中.不正确的是( )| A. |  | B. |  | C. | 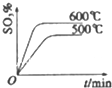 | D. |  |
分析 已知2SO2(g)+O2(g)?2SO3(g)△H=-196kJ•mol-1,该反应正方向为:体积减小,放热反应;结合温度、压强对速率和平衡的影响分析.
解答 解:已知2SO2(g)+O2(g)?2SO3(g)△H<0,该反应正方向为:体积减小,放热反应;
A、升高温度平衡逆移,所以逆速率大于正速率,与图象相符,故A正确;
B、随着反应进行三氧化硫的含量逐渐增大,当达到平衡时,再升高温度,平衡逆移,所以三氧化硫含量减小,与图象相符,故B正确;
C、升高温度,平衡逆移,所以三氧化硫含量减小,温度高反应速率快,达到平衡所需时间短,所以600℃的曲线应该在下面,故C错误;
D、该反应正方向为:体积减小的方向,增大压强,平衡正移,三氧化硫的含量增大,所以压强大的曲线在上面,故D正确;
故选C.
点评 本题考查了温度、压强对速率和平衡的影响等知识点,难度较大,掌握移动原理是解题关键.

练习册系列答案
相关题目
7.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理.
(1)提出假设
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为Mg(OH)2 .
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
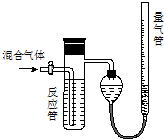
(3)为进一步确定实验I的产物,设计定量实验方案,如图所示:
称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 .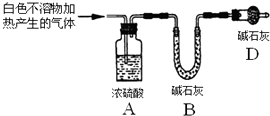
(1)提出假设
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为Mg(OH)2 .
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为 氢气 |
| 实验Ⅲ | 取实验I中的白色不溶物,洗涤, 加入足量稀盐酸 | 产生气泡沉淀全部溶解 | 白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验I中的澄清液,向其中加 入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在④ CO32-离子 |
称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中.实验前后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 .

12.碘在不同状态下(固态或气态)与氮气反应的热化学方程式如下所示:
①H2(g)+I2(?)?2HI(g)△H=+9.48kJ•mol-1
②H2(g)+I2(?)?2HI(g)△H=-26.48kJ•mol-1
下列刘断正确的是( )
①H2(g)+I2(?)?2HI(g)△H=+9.48kJ•mol-1
②H2(g)+I2(?)?2HI(g)△H=-26.48kJ•mol-1
下列刘断正确的是( )
| A. | ①中的为气态.②中的为固态 | |
| B. | ①的反应物总能量比②的反应物总能量低 | |
| C. | ①的产物比反应②的产物热稳定性更好 | |
| D. | 1mol固态碘升华时将吸热17kJ |
9.下列对氧化还原反应的分析中不合理的是( )
| A. | Mg变为MgO时化合价升高,故Mg在该反应中作还原剂 | |
| B. | 在反应2H2S+SO2═3S+2H2O中,氧化产物和还原产物都是S | |
| C. | 凡是置换反应都是氧化还原反应 | |
| D. | 在反应2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑中,H2是还原剂 |
7.下列关于${\;}_{49}^{115}$In的说法中,错误的是( )
| A. | ${\;}_{49}^{115}$In原子核外有49个电子 | |
| B. | ${\;}_{49}^{115}$In是In元素的一种核素 | |
| C. | ${\;}_{49}^{115}$In原子核内质子数和中子数之差等于17 | |
| D. | ${\;}_{49}^{115}$In原子核内有49个中子 |

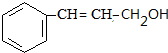 .
.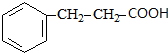 +
+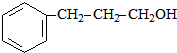 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$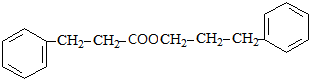 +H2O.
+H2O.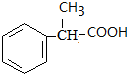 .
.