题目内容
20.下列化学方程式中不正确的是( )| A. | CH3CH2CH2OH+HBr$→_{H+}^{△}$CH3CH2CH2Br+H2O | |
| B. | 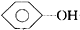 +NaHCO3→ +NaHCO3→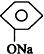 +H2CO3 +H2CO3 | |
| C. | 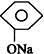 +CO2+H2O→ +CO2+H2O→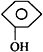 +NaHCO3 +NaHCO3 | |
| D. |  +3Br2→ +3Br2→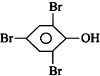 ↓+3HBr ↓+3HBr |
分析 A.醇可被HBr在酸性条件下取代;
B.苯酚酸性比碳酸弱;
C.碳酸酸性比苯酚强,但苯酚酸性比+NaHCO3强;
D.苯酚可与溴水发生取代反应.
解答 解:A.CH3CH2CH2OH可被HBr在酸性条件下取代生成CH3CH2CH2Br,方程式为CH3CH2CH2OH+HBr$→_{H+}^{△}$CH3CH2CH2Br+H2O,故A正确;
B.苯酚酸性比碳酸弱,不能生成碳酸,故B错误;
C.碳酸酸性比苯酚强,但苯酚酸性比+NaHCO3强,发生 +CO2+H2O→
+CO2+H2O→ +NaHCO3,故C正确;
+NaHCO3,故C正确;
D.苯酚可与溴水发生取代反应生成三溴苯酚,方程式为 +3Br2→
+3Br2→ ↓+3HBr,故D正确.
↓+3HBr,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,难度不大.

练习册系列答案
相关题目
2.下列表述中,合理的是( )
| A. | 准确量取20.00mL高锰酸钾溶液,可选用25 mL碱式滴定管 | |
| B. | 将水加热,Kw增大,pH不变 | |
| C. | 用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 mol电子转移时,阴极析出6.4g金属 | |
| D. | CuSO4 的水溶液经加热浓缩、蒸干灼烧后能得到CuSO4固体 |
15.硝酸铜是制备Cu-Zn-Al系催化剂的重要原料.现有三种制取硝酸铜的实验方案可供选用:
①铜与稀硝酸反应制取:3Cu+8HNO3(稀)$\frac{\underline{\;\;△\;\;}}{\;}$3Cu(NO3)2+2NO↑+4H2O
②铜与浓硝酸反应制取:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,CuO+2HNO3═Cu(NO3)2+H2O
下列说法正确的是( )
①铜与稀硝酸反应制取:3Cu+8HNO3(稀)$\frac{\underline{\;\;△\;\;}}{\;}$3Cu(NO3)2+2NO↑+4H2O
②铜与浓硝酸反应制取:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,CuO+2HNO3═Cu(NO3)2+H2O
下列说法正确的是( )
| A. | 制取等量的硝酸铜,需硝酸的量②最少 | |
| B. | 制取等量的硝酸铜,②产生的有毒气体比①少 | |
| C. | 三种方案中,硝酸的利用率为③>①>② | |
| D. | 三种方案的反应都可以在铁质容器中进行 |
5.下列离子方程式书写正确的是( )
| A. | Ba(OH)2溶液与稀H2SO4反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 往FeCl3溶液中加入Cu粉:Fe3++Cu═Fe2++Cu2+ | |
| C. | Al(OH)3沉淀中滴加盐酸 Al(OH)3+3H+═Al3++3H2O | |
| D. | FeCl2溶液中通入Cl2:2Fe2++Cl2═2Fe3++2Cl- |
10.某稀溶液中含4mol KNO3和2.5mol H2SO4,向其中加入1.5mol Fe粉,充分反应后产生的NO气体在标准状况下的体积为( )
| A. | 36 L | B. | 28 L | C. | 22.4 L | D. | 11.2 L |
 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行了有关实验:
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行了有关实验: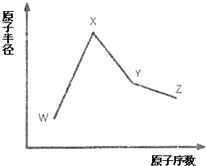 W、X、Y和Z是常见的短周期元素,其原子半径随原子序数变化如图所示.己知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.
W、X、Y和Z是常见的短周期元素,其原子半径随原子序数变化如图所示.己知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小. .
.