��Ŀ����
16��2013��6�£��ҹ������������ٴ�ˢ�¡��й���ȡ�--��DZ7062�ף�Ϊ�ҹ��������Դ�Ŀ����춨�˻�����������зḻ���̽�˿��̽�˵���Ҫ�ɷ���MnO2��ͬʱ�����л�ͭ�������������������������ѺϽ�����Ƴɣ���������7000m����г�����ѹ��Ti�����Ѱۣ�TiO2��Ϊԭ�Ͻ����������Ѱ�������TiO2+����ˮ���������ᣨH2TiO3�������������ճ����Ƶõģ�TiO2+����ˮ������ӷ���ʽΪTiO2++2H2O=H2TiO3��+2H+��
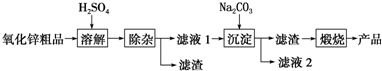
��MnO2��һ����Ҫ�������ܲ��ϣ���ҵ�ϴ��̽������ȡ������MnO2����������ͼ��ʾ��
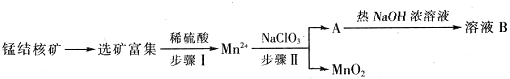
��1�����������NaClO3Ϊ��������������0.05molMnO2ʱ������0.1mol/L��NaClO3��Һ200ml���÷�Ӧ���ӷ���ʽΪ2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2����
��2����֪��ҺB������֮һ��ѭ���������������������ʵ������������ƣ�
�����û�ͭ����ͭ������¯������Fe2O3��FeO��SiO2��Al2O3�ȣ����Ʊ�Fe2O3������Ϊ��
��A���ù�����ϡ�����ȡ¯�������ˣ�
��B������Һ�м���5%��H2O2���������м��������NaOH��Һ�����ˣ�������ϴ�ӡ�������յõ�Fe2O3
����������Ϣ�ش��������⣺
��1����B��������Һ�м���5%��H2O2����Ŀ���������������ӣ�
��2�����ʵ��֤��¯���к���FeOȡ¯����������ϡ�����ȡ�����ҺʹKMnO4��Һ��ɫ��
��3�������յõ���Fe2O3��ԭΪFe���ʣ��ٽ�����Ϊm g��Fe���ʷֳ���ȵ��ķݣ��ֱ���50mL��100mL��150mL��200mL�ĵ�Ũ�ȵ�ϡ���ᷴӦ����Ӧ����NO�ڱ���µ������������
| ʵ�� | �� | �� | �� | �� |
| V��HNO3��/mL | 50 | 100 | 150 | 200 |
| V��NO��/L | 1.344 | 2.688 | 3.36 | 3.36 |
���� ��TiO2+����ˮ���������ᣨH2TiO3�������������ԭ���غ��֪�����������Ӳ�����
��1��0.1mol/L��NaClO3��Һ200ml�����ʵ�����0.02mol��������0.05molMnO2ʱ��ת�Ƶ��ӵ����ʵ�����0.05mol����4-2��=0.1mol�����ݵ��ӵ�ʧ�غ��֪0.02mol�����Ƶõ�0.1mol���ӣ������Ԫ�صĻ��ϼ۱仯5�ۣ�����+5�۽��͵�0�ۣ���˻�ԭ��������������2���������ȵ�����������Һ��Ӧ���������ơ��Ȼ��ƺ�ˮ��
��1��˫��ˮ�������Խ�������������Ϊ�����ӣ�
��2���������Ӿ��л�ԭ�ԣ�
��3���ٸ��ݱ������ݿ�֪ʵ��ۺ������ǹ����ģ�����������ϡ���ᷴӦ�������3.36LNO��NO�����ʵ�����0.15mol����Ӧ��ת�Ƶ��ӵ����ʵ�����0.15mol����5-2��=0.45mol����˸��ݵ��ӵ�ʧ�غ��֪�����������ʵ�����$\frac{0.45mol}{3}$=0.15mol�����ԭ�������ʵ�����0.15mol��4=0.6mol��
��ʵ����в���NO�����ʵ�����$\frac{2.688L}{22.4L/mol}$=0.12mol��ת�Ƶ��ӵ����ʵ�����0.36mol�����������������������������ʵ�����xmol��ymol����x+y=0.15��3x+2y=0.36�����x=0.06��y=0.09�������������������������ʵ���֮����2��3��
��� �⣺��TiO2+����ˮ���������ᣨH2TiO3�������������ԭ���غ��֪�����������Ӳ��������TiO2+����ˮ������ӷ���ʽΪTiO2++2H2O=H2TiO3��+2H+��
�ʴ�Ϊ��TiO2++2H2O=H2TiO3��+2H+��
��1��0.1mol/L��NaClO3��Һ200ml�����ʵ�����0.02mol��������0.05molMnO2ʱ��ת�Ƶ��ӵ����ʵ�����0.05mol����4-2��=0.1mol�����ݵ��ӵ�ʧ�غ��֪0.02mol�����Ƶõ�0.1mol���ӣ������Ԫ�صĻ��ϼ۱仯5�ۣ�����+5�۽��͵�0�ۣ���˻�ԭ���������������Ը÷�Ӧ���ӷ���ʽΪ2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2����
�ʴ�Ϊ��2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2����
��2���������ȵ�����������Һ��Ӧ���������ơ��Ȼ��ƺ�ˮ����˿���ѭ��������B�������ƣ�
�ʴ�Ϊ�������ƣ�
��1����Һ�к����������ӣ�˫��ˮ�������Խ�������������Ϊ�����ӣ��Ҳ��������µ����ʣ�
�ʴ�Ϊ�������������ӣ�
��2���������Ӿ��л�ԭ�ԣ���˼���¯���к���FeO��ʵ�鷽����ȡ¯����������ϡ�����ȡ�����ҺʹKMnO4��Һ��ɫ��
�ʴ�Ϊ��ȡ¯����������ϡ�����ȡ�����ҺʹKMnO4��Һ��ɫ��
��3���ٸ��ݱ������ݿ�֪ʵ��ۺ������ǹ����ģ�����������ϡ���ᷴӦ�������3.36LNO��NO�����ʵ�����$\frac{3.36L}{22.4L/mol}$=0.15mol����Ӧ��ת�Ƶ��ӵ����ʵ�����0.15mol����5-2��=0.45mol����˸��ݵ��ӵ�ʧ�غ��֪�����������ʵ�����$\frac{0.45mol}{3}$=0.15mol�����ԭ�������ʵ�����0.15mol��4=0.6mol��������0.6mol��56g/mol=33.6g��
�ʴ�Ϊ��33.6��
��ʵ����в���NO�����ʵ�����$\frac{2.688L}{22.4L/mol}$=0.12mol��ת�Ƶ��ӵ����ʵ�����0.36mol�����������������������������ʵ�����xmol��ymol����
x+y=0.15
3x+2y=0.36
���x=0.06��y=0.09��
�����������������������ʵ���֮����2��3��������Һ��Fe2+��Fe3+���ʵ���֮��Ϊ3��2��
�ʴ�Ϊ��3��2��
���� ���⿼�����ݽ϶࣬�������ˮ�⡢���ӷ���ʽ����д���Ʊ�ʵ�鷽������Ƶ�֪ʶ��������ѧ���ķ���������ʵ�������Ŀ��飬Ϊ�߿��������ͣ�ע�����֪ʶ��ѧϰ����ۣ��ѶȲ���

| A�� | 0.4 mol | B�� | 0.5 mol | C�� | 0.6 mol | D�� | 0.8 mol |
| A�� | �������ϩ | B�� | ����ͱ�ϩ | C�� | �������ϩ | D�� | ����ͱ�ϩ |
| A�� | �����л�����ϩ��ͨ��������һ�������·�Ӧ��ʹ��ϩת��Ϊ���� | |
| B�� | �ؽᾧ���ᴿ������ʱ��Ϊ�˳�ȥ���ʺͷ�ֹ������������Ӧ�ó��ȹ��� | |
| C�� | ����������Һʱ������������Һ��������ϡ��ˮ�У���������������μӵ������պ��ܽ�Ϊֹ | |
| D�� | ��ˮ�Ҵ���Ũ���Ṳ�ȵ�170�棬���Ƶõ�����ͨ�����Ը�����ؿɼ����Ƶõ������Ƿ�Ϊ��ϩ |
| A�� | Z��Ũ��Ϊ0.4 mol•L-1 | B�� | X2��Z��Ũ�Ⱦ�Ϊ0.15 mol•L-1 | ||
| C�� | X2��Z��Ũ��֮��Ϊ0.4 mol•L-1 | D�� | X2��Ũ��Ϊ0.4 mol•L-1 |
| A�� | 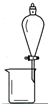 ��CCl4��ȡ��ˮ�е�Br2 ��CCl4��ȡ��ˮ�е�Br2 | B�� |  ��KI��I2�Ĺ��������л���I2 ��KI��I2�Ĺ��������л���I2 | ||
| C�� | 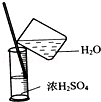 ϡ��Ũ���� ϡ��Ũ���� | D�� | 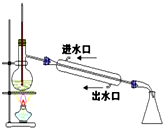 ��ҵ�ƾ��Ʊ���ˮ�ƾ� ��ҵ�ƾ��Ʊ���ˮ�ƾ� |
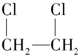 ������ķ����ǣ�������
������ķ����ǣ�������| A�� | CH3CH3��Cl2ȡ�� | B�� | CH2�TCH2��HCl�ӳ� | ||
| C�� | CH2�TCH2��Cl2�ӳ� | D�� | CH3CH2Cl��Cl2ȡ�� |