题目内容
8.完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )| A. | 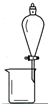 用CCl4提取溴水中的Br2 用CCl4提取溴水中的Br2 | B. |  从KI和I2的固体混合物中回收I2 从KI和I2的固体混合物中回收I2 | ||
| C. | 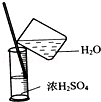 稀释浓硫酸 稀释浓硫酸 | D. | 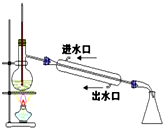 工业酒精制备无水酒精 工业酒精制备无水酒精 |
分析 A.用CCl4提取溴水中的Br2,应该采用萃取方法,需要的仪器有分液漏斗、烧杯;
B.碘单质易升华;
C.量筒只能量取溶液,不能溶解或稀释药品,且稀释浓硫酸时应该将浓硫酸倒入水中;
D.蒸馏时温度计测量馏分温度,且冷凝管中上口是出水口、下口是进水口.
解答 解:A.用CCl4提取溴水中的Br2,应该采用萃取方法,需要的仪器有分液漏斗、烧杯,符合条件,故A正确;
B.加热后,碘单质易升华,剩余的是KI,采用该方法得不到碘单质,故B错误;
C.量筒只能量取溶液但不能溶解或稀释药品,要稀释浓硫酸需要烧杯,且稀释浓硫酸时应该将浓硫酸倒入水中,防止溅出液体而产生安全事故,故C错误;
D.乙醇和水互溶,应该采用蒸馏方法分离,蒸馏时温度计测量馏分温度,且冷凝管中上口是出水口、下口是进水口,故D错误;
故选A.
点评 本题考查实验方案评价,涉及基本操作、仪器的选取等知识点,明确实验原理及基本操作规范性是解本题关键,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
18.下列关于铁的叙述正确的是( )
①铁能被磁铁吸引,但纯铁比含杂质的铁易被腐蚀
②在人体的血红蛋白中含有铁元素
③铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
④铁与强氧化剂硝酸反应的产物只有一种是Fe(NO3)3
⑤不能通过化合反应制得FeCl2和Fe(OH)3.
①铁能被磁铁吸引,但纯铁比含杂质的铁易被腐蚀
②在人体的血红蛋白中含有铁元素
③铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
④铁与强氧化剂硝酸反应的产物只有一种是Fe(NO3)3
⑤不能通过化合反应制得FeCl2和Fe(OH)3.
| A. | ①③ | B. | ②③ | C. | ②⑤ | D. | ④⑤ |
19.为了增强环保意识,变废为宝,我国多个城市实行垃圾分类回收.通常,绿色箱用来装可回收再利用垃圾,黄色箱用来装不可回收垃圾.以下物质能扔进绿色垃圾箱的是( )
①废旧报纸
②废铜钱
③一次性塑料盒
④口香糖渣
⑤果皮
⑥空矿泉水瓶
⑦废铁锅.
①废旧报纸
②废铜钱
③一次性塑料盒
④口香糖渣
⑤果皮
⑥空矿泉水瓶
⑦废铁锅.
| A. | ①③⑤⑦ | B. | ③④⑤⑥ | C. | ①②⑤⑦ | D. | ①②⑥⑦ |
16.2013年6月,我国“蛟龙”号再次刷新“中国深度”--下潜7062米,为我国深海矿物资源的开发奠定了基础.海洋深处有丰富的锰结核矿,锰结核的主要成分是MnO2,同时还含有黄铜矿.
Ⅰ、“蛟龙”号外壳是用特殊的钛合金材料制成,它可以在7000m的深海中承受重压,Ti是以钛白粉(TiO2)为原料进行生产,钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的.TiO2+发生水解的离子方程式为TiO2++2H2O=H2TiO3↓+2H+.
Ⅱ、MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:
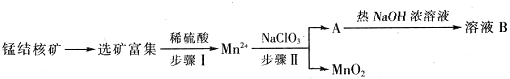
(1)步骤Ⅱ中以NaClO3为氧化剂,当生成0.05molMnO2时,消耗0.1mol/L的NaClO3溶液200ml,该反应离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑.
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是氯酸钠.
Ⅲ、利用黄铜矿炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)可制备Fe2O3,方法为:
(A)用过量的稀盐酸浸取炉渣、过滤;
(B)向滤液中加入5%的H2O2,再向其中加入过量的NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得到Fe2O3
根据以上信息回答下列问题:
(1)(B)中向滤液中加入5%的H2O2,其目的是氧化亚铁离子.
(2)设计实验证明炉渣中含有FeO取炉渣少许,用稀硫酸浸取后的溶液使KMnO4溶液褪色.
(3)将煅烧得到的Fe2O3还原为Fe单质,再将质量为m g的Fe单质分成相等的四份,分别与50mL、100mL、150mL、200mL的等浓度的稀硝酸反应,反应产物NO在标况下的体积见附表:
则:①m=33.6g ②写出实验②发生反应后溶液中Fe2+与Fe3+物质的量之比为:3:2.
Ⅰ、“蛟龙”号外壳是用特殊的钛合金材料制成,它可以在7000m的深海中承受重压,Ti是以钛白粉(TiO2)为原料进行生产,钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的.TiO2+发生水解的离子方程式为TiO2++2H2O=H2TiO3↓+2H+.
Ⅱ、MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:
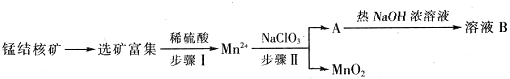
(1)步骤Ⅱ中以NaClO3为氧化剂,当生成0.05molMnO2时,消耗0.1mol/L的NaClO3溶液200ml,该反应离子方程式为2ClO3-+5Mn2++4H2O=5MnO2+8H++Cl2↑.
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是氯酸钠.
Ⅲ、利用黄铜矿炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)可制备Fe2O3,方法为:
(A)用过量的稀盐酸浸取炉渣、过滤;
(B)向滤液中加入5%的H2O2,再向其中加入过量的NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得到Fe2O3
根据以上信息回答下列问题:
(1)(B)中向滤液中加入5%的H2O2,其目的是氧化亚铁离子.
(2)设计实验证明炉渣中含有FeO取炉渣少许,用稀硫酸浸取后的溶液使KMnO4溶液褪色.
(3)将煅烧得到的Fe2O3还原为Fe单质,再将质量为m g的Fe单质分成相等的四份,分别与50mL、100mL、150mL、200mL的等浓度的稀硝酸反应,反应产物NO在标况下的体积见附表:
| 实验 | ① | ② | ③ | ④ |
| V(HNO3)/mL | 50 | 100 | 150 | 200 |
| V(NO)/L | 1.344 | 2.688 | 3.36 | 3.36 |
3.下列有关电化学装置完全正确的是( )
| A. |  铜的冶炼 | B. | 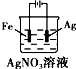 铁上镀银 | C. |  防止Fe被腐蚀 | D. |  构成铜锌原电池 |
20.下列有关安全问题的叙述不正确的是( )
| A. | 工业制取硝酸时尾气用氢氧化钠溶液吸收 | |
| B. | 氯气泄露时,应用蘸有肥皂水的湿毛巾捂住口鼻到安全区域 | |
| C. | 家中做卫生保洁时,严禁漂白粉与浓盐酸混合使用,否则会产生有毒气体 | |
| D. | 家中发生天然气泄露时,应立即使用室内电话报警 |

 .
.