题目内容
18.下列关于苯酚的叙述中,错误的是( )| A. | 其水溶液显酸性,俗称石碳酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后立即放出二氧化碳 |
分析 A、苯酚水溶液显弱酸性,俗称石炭酸;
B、苯酚若不慎沾在皮肤上,应立即用酒精擦洗;
C、苯酚在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶;
D、苯酚酸性小于碳酸酸性,不会生成二氧化碳气体.
解答 解:A、苯酚的水溶液显弱酸性,俗称石炭酸,故A正确;
B、苯酚有腐蚀性,苯酚若不慎沾在皮肤上,应立即用酒精擦洗,因为苯酚易溶于乙醇,乙醇五毒且乙醇具有挥发性,故B正确;
C、苯酚在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶,故C正确;
D、由于苯酚酸性小于碳酸酸性,在碳酸氢钠溶液中滴入苯酚的水溶液,不会生成二氧化碳气体,故D错误.
故选D.
点评 本题主要考查学生苯酚的物理性质以及化学性质,注意碳酸酸性与苯酚酸性强弱的比较,属于基本知识的考查,较简单.

练习册系列答案
相关题目
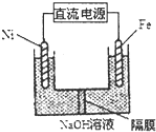
9.500mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol•L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
| A. | 原混合溶液中c(K+)为4 mol•L-1 | |
| B. | 上述电解过程中共转移4 mol电子 | |
| C. | 电解得到的Cu的物质的量为0.5 mol | |
| D. | 电解后溶液中c(H+)为2 mol•L-1 |
6.在标准状况下,在三个干燥的烧瓶内分别装有干燥、纯净的NH3;含一半空气的氯化氢气体;NO2和O2体积比为4:1的混合气体.然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为( )
| A. | 2:1:2 | B. | 5:5:4 | C. | 1:1:1 | D. | 无法确定 |
13.原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,Y能分别与X、Z形成原子个数比为1:3的化合物,常温下YX3是一种刺激性气味的气体.下列说法正确的是( )
| A. | 原子半径:Z<Y<W,而离子半径:W<Y<Z | |
| B. | W的氯化物水溶液中滴加过量NaZ饱和溶液,可生成W的配合物用于冶金工业 | |
| C. | 由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度大于酸根离子浓度 | |
| D. | 已知YX3沸点远高于YZ3,则Y-X键的键能高于Y-Z键 |
10.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 沸点高的物质制备沸点低的物质 | 钙置换出铷,或浓磷酸制备HI |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | BCl3沸点低于AlCl3,CO2沸点低于SiO2 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
| A. | A | B. | B | C. | C | D. | D |
7.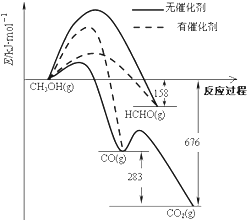 如图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].下列说法不正确的是( )
如图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].下列说法不正确的是( )
 如图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].下列说法不正确的是( )
如图所示为一定条件下1molCH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].下列说法不正确的是( )| A. | 未使用催化剂,氧化产物有三种 | |
| B. | 使用催化剂,氧化产物主要是CO或者HCHO | |
| C. | CH3OH的燃烧热大于676kJ•mol-1 | |
| D. | 2HCHO(g)+O2=2CO(g)+2H2O(g)△H=-470kJ•mol-1 |
8.已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4 mol•L-1的Na2CO3溶液与CaCl2溶液等体积混合,若要产生沉淀,则所用CaCl2溶液的浓度至少应为( )
| A. | 2.8×10-2 mol•L-1 | B. | 1.4×10-5 mol•L-1 | ||
| C. | 2.8×10-5 mol•L-1 | D. | 5.6×10-5 mol•L-1 |
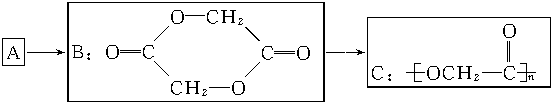
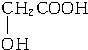 .
. .
.