题目内容
8.医用化学杂志曾报道,有一种功能高分子材料为聚乙交酯纤维材料C,用这种功能高分子材料制成手术缝合线比天然高分子材料的肠线好.它的合成过程如图所示: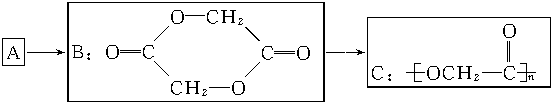
(1)写出A的结构简式
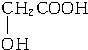 .
.(2)写出由A制取B的化学方程式
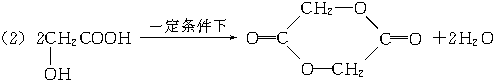 .
.(3)可用作医用的高分子材料须具备哪些性能?
分析 据B的结构简式可知A→B是酯化反应,则A为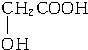 ,B→C是聚合反应,生成的高分子聚乙交酯纤维材料具有,优异的生物相容性,较少受到排斥,无毒性,具有很高的机械性能以及其他一些特殊性能,据此分析.
,B→C是聚合反应,生成的高分子聚乙交酯纤维材料具有,优异的生物相容性,较少受到排斥,无毒性,具有很高的机械性能以及其他一些特殊性能,据此分析.
解答 解:(1)据B的结构简式可知A→B是酯化反应,则A为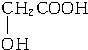 ,故答案为:
,故答案为: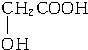 ;
;
(2)A→B是在浓硫酸作用下的酯化反应,反应方程式为: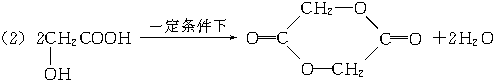 ,
,
故答案为: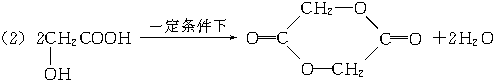 ;
;
(3)高分子聚乙交酯纤维材料具有,优异的生物相容性,较少受到排斥,无毒性,具有很高的机械性能以及其他一些特殊性能,故答案为:优异的生物相容性,较少受到排斥,无毒性,具有很高的机械性能以及其他一些特殊性能.
点评 本题考查有机物的推断,需要对给予的反应信息进行利用能较好的考查考生的阅读、自学能力和思维能力,是热点题型,注意掌握官能团的性质与转化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.工业上制取氧气的主要方法是( )
| A. | 加热氯酸钾 | B. | 加热高锰酸钾 | C. | 电解水 | D. | 分离空气 |
19.某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿氏常数,下列说法中正确的是( )
| A. | 氧元素的相对原子质量为$\frac{12a}{b}$ | B. | 1mol该原子质量为aNAg | ||
| C. | x g该氧原子所含的电子数为$\frac{8x}{a}$ | D. | y g 该氧原子的中子数一定为$\frac{8y}{a}$ |
13.下列离子方程式中,不正确的是( )
| A. | C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| B. | C6H5OH+OH-→C6H5O-+H2O | |
| C. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O |
17.碳及其化合物在工农业生产生活中有着重要作用.请按要求回答下列问题:

(1)已知:C(s)+O2(g)=CO2(g)△H=-393kJ•mol-1;
2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-484kJ•mol-1
将水蒸气喷到灼热的炭上可实现炭的气化(制得CO、H2),该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g),△H=+132kJ•mol-1.
(2)将一定量CO(g)和H2O(g)分别通入容积为2L的恒容密闭容器中,一定条件下发生反应为CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组实验数
①该反应的正反应为放热(填“吸热”或“放热”)反应.
②实验1中,0~4min时段内,以v(H2)表示的反应速率为0.4mol/(L•min).若在此温度下H2O(g)、CO(g)起始量分别为2mol、4mol,则此反应的平衡常数为$\frac{8}{3}$.
③实验2达到平衡时CO的转化率为20%.
④实验3与实验2相比,改变的条件是加催化剂;
请在如图1坐标中画出“实验2”与“实验3”中c(CO2)随时间变化的曲线,并作标注实验编号.
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池的负极反应式为CH3OH-6e-+8OH-═CO32-+6H2O.
(4)一定条件下,如图2示装置可实现有机物的电化学储氢(忽略其它有机物),则阴极的电极反应式为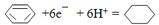 .
.

(1)已知:C(s)+O2(g)=CO2(g)△H=-393kJ•mol-1;
2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-484kJ•mol-1
将水蒸气喷到灼热的炭上可实现炭的气化(制得CO、H2),该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g),△H=+132kJ•mol-1.
(2)将一定量CO(g)和H2O(g)分别通入容积为2L的恒容密闭容器中,一定条件下发生反应为CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组实验数
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
②实验1中,0~4min时段内,以v(H2)表示的反应速率为0.4mol/(L•min).若在此温度下H2O(g)、CO(g)起始量分别为2mol、4mol,则此反应的平衡常数为$\frac{8}{3}$.
③实验2达到平衡时CO的转化率为20%.
④实验3与实验2相比,改变的条件是加催化剂;
请在如图1坐标中画出“实验2”与“实验3”中c(CO2)随时间变化的曲线,并作标注实验编号.
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池的负极反应式为CH3OH-6e-+8OH-═CO32-+6H2O.
(4)一定条件下,如图2示装置可实现有机物的电化学储氢(忽略其它有机物),则阴极的电极反应式为
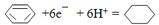 .
.
18.下列关于苯酚的叙述中,错误的是( )
| A. | 其水溶液显酸性,俗称石碳酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后立即放出二氧化碳 |
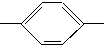 CH═N
CH═N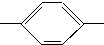 CH2CH2CH2CH3 MBBA
CH2CH2CH2CH3 MBBA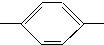 CHO 醛A
CHO 醛A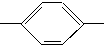 NH2 胺B
NH2 胺B NH2、CH3CH2CH2CH2
NH2、CH3CH2CH2CH2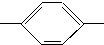 NH2、CH3CH2CH(CH3)
NH2、CH3CH2CH(CH3)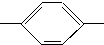 NH2、(CH3)3C
NH2、(CH3)3C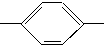 NH2.
NH2.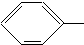 COOCH3、
COOCH3、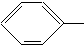 OOCCH3、HCOO
OOCCH3、HCOO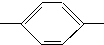 CH3、
CH3、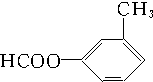 、
、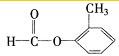 、
、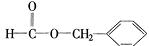 .
.