题目内容
【题目】25 ℃时,x mol·L-1氢氟酸水溶液中,加入KOH固体调节溶液的pH(忽略加入固体引起的溶液体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示。下列说法正确的是 ( )。

A.当c(F-)>c(HF)时,溶液呈碱性
B.当pH=2时,c(F-)<c(K+)
C.25 ℃时,氢氟酸的电离平衡常数为4×10-6
D.当pH=5时,c(HF)+c(K+)+c(H+)-c(OH-)=x mol·L-1
【答案】D
【解析】
A、根据图像可以得出当c(F-)>c(HF)时,溶液也可以呈酸性;
B、由电荷守恒得,c(K+)+c(H+)=c(F-)+c(OH-),当pH=2时,c(H+)>c(OH-),则c(F-)>c(K+)时才满足电荷守恒;
C、Ka=![]() ,由图像可知两曲线交点时c(F-)=c(HF),pH约为3;即c(H+)=10-3 mol·L-1所以Ka=c(H+)=10-3,所以C项不正确;
,由图像可知两曲线交点时c(F-)=c(HF),pH约为3;即c(H+)=10-3 mol·L-1所以Ka=c(H+)=10-3,所以C项不正确;
D、根据电荷守恒,得c(K+)+c(H+)=c(F-)+c(OH-),若两边均加上c(HF),可得c(HF)+c(K+)+c(H+)=c(F-)+c(OH-)+c(HF),移项可得c(HF)+c(K+)+c(H+)-c(OH-)=c(F-)+c(HF),忽略加入固体引起的溶液体积变化,得c(F-)+c(HF)=x mol·L-1。

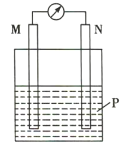
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,其中P为电解质溶液。由此判断M、N、P所代表的物质可能是( )
选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 锌 | 稀硫酸 |
C | 银 | 锌 | AgNO3溶液 |
D | 铜 | 铁 |
|
A.AB.BC.CD.D
【题目】某温度时,在10L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化下表中数据
t/min | X/mol | Y/mol | Z/mol |
0 | 1.00 | 2.00 | 0.00 |
1 | 0.90 | 1.80 | 0.20 |
3 | 0.75 | 1.50 | 0.50 |
5 | 0.65 | 1.30 | 0.70 |
9 | 0.55 | 1.10 | 0.90 |
10 | 0.55 | 1.10 | 0.90 |
14 | 0.55 | 1.10 | 0.90 |
(1)体系中发生反应的化学方程式____________;
(2)列式计算该反应在0~3 min时间内产物Z的平均反应速率:________;
(3)该反应达到平衡时反应物X的转化率α等于________;
(4)如果该反应是放热反应,改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1____________,2______________,3______________。