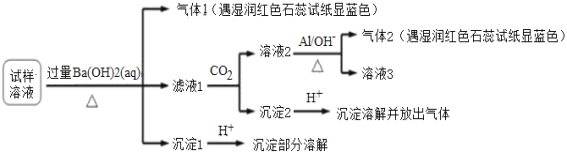
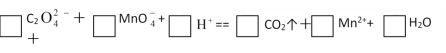题目内容
【题目】硫酸性质是中学化学学习的重点。请回答下列问题:
(1)中学化学中利用物质与浓硫酸共热可制备SO2气体,写出用浓硫酸还可制备不同类别的气体的名称:_____________________写一种)。
(2)某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用下图所示装置进行有关实验。

①装置B的作用是贮存多余的气体。B中应放置的液体是_______(填序号)
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
②反应完毕后,烧瓶中还有一定量的余酸,使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是____(填序号)。
a.Fe粉 b.BaCl2溶液 c.CuO d.Na2CO3溶液
③实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该反应的化学方程式是_________。
④为验证二氧化硫的还原性,C中盛有氯水,充分反应后,取C中的溶液分成三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是___(填“I”、“Ⅱ”或“Ⅲ”);C中发生反应的离子方程式为____________。D中盛有氢氧化钠溶液,当通入二氧化硫至试管D中溶液显中性时,该溶液中c(Na+)=______(用含硫微粒浓度的代数式表示)。
(3)利用FeCl3溶液的氧化性也可以吸收SO2。该反应的离子方程式是_____________。检验FeCl3是否完全被还原的方法为______________________。
【答案】乙烯db2Cu+2H2SO4 +O2=2CuSO4+2H2OⅢ合理Cl2+SO2+2H2O=4H++2Cl-+SO42-c(Na+)=2c(SO32-)+c(HSO3-)2Fe3++SO2+2H2O=2Fe2++ SO42-+4H+取少量反应后的溶液滴加少量硫氰化钾溶液,若不变红则氯化铁完全被还原
【解析】
(1)利用乙醇在浓硫酸加热条件下发生消去反应制备乙烯。(2)①装置B的作用是贮存多余的二氧化硫气体,所以B中应放置的液体应不与二氧化硫反应,亚硫酸钠溶液可以和二氧化硫反应,二氧化硫能使酸性高锰酸钾溶液或溴水褪色,但是其不与亚硫酸氢钠反应。虽然二氧化硫易溶于水,但是其在饱和亚硫酸氢钠溶液中的溶解度很小,所以选择饱和亚硫酸氢钠溶液,即选d。②反应后剩余的酸为硫酸,溶液还有硫酸铜,利用与氢离子的反应进行检验,氧化铜、铁、碳酸钠都能与硫酸反应且有明显的现象,而氯化钡与硫酸、硫酸铜均可反应生成白色沉淀,故不能证明有硫酸剩余的是氯化钡溶液,选b。(3)向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,通入的气体具有氧化性,根据元素守恒可知,应通入氧气,反应方程式为2Cu+2H2SO4 +O2=2CuSO4+2H2O。(4)氯水与二氧化硫反应生成氯化氢和硫酸,检验反应后溶液中含有硫酸根离子,说明二氧化硫具有还原性。氯水溶液中含有氯离子,能与硝酸银生成白色沉淀,所以方案Ⅰ不合理,氯水中含有次氯酸,可以使品红溶液褪色,不能说明二氧化硫还原性,方案Ⅱ不合理,向第三份溶液加入氯化钡溶液,产生白色沉淀,说明生成硫酸根离子,方案Ⅲ合理。 C中发生反应的离子方程式为:Cl2+SO2+2H2O=4H++2Cl-+SO42-;根据电荷守恒分析,D中溶液显中性时溶液中有 c(Na+)=2c(SO32-)+c(HSO3-) (3)在溶液中铁离子将二氧化硫氧化为硫酸,反应离子方程式为 2Fe3++SO2+2H2O=2Fe2++ SO42-+4H+;检验氯化铁是否完全被还原的方法为:取少量反应后的溶液滴加少量硫氰化钾溶液,若不变红则氯化铁完全被还原。