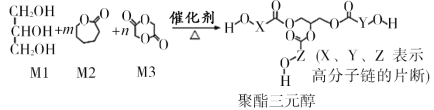
ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩ”…œ¬Ν– Β―ιœ÷œσ“ΜΕ®ΡήΒΟ≥ωœύ”ΠΫα¬έΒΡ «
―Γœν | A | B | C | D |
ΉΑ÷ΟΜρ≤ΌΉς | »ΓΝΫ÷ß ‘ΙήΗςΦ”»κ4 mL 0.01 mol/LΒΡ≤ίΥα»ή“ΚΘ§Ζ÷±πΒΈΦ”2 mL 0.1 mol/LΓΔ0.2 mol/LΒΡΗΏΟΧΥαΦΊ»ή“Κ |
|
| œρΖ÷±π Δ”–5 mL 0.1 mol/LΒΡΝρ¥ζΝρΥαΡΤ»ή“ΚΒΡ ‘Ιή÷–ΒΈΦ”5 mL 0.1 mo/LΒΡΝρΥα»ή“ΚΘ§“ΜΕΈ ±ΦδΚσΘ§Ζ÷±πΖ≈‘ΎάδΥ°ΚΆ»»Υ°÷–ΓΘ |
œ÷œσ | Ά …Ϊ≤ΔΙέ≤λΆ …ΪΒΡ ±Φδ | Ήσ±ΏΟό«ρ±δΜΤΘ§”“±ΏΟό«ρ±δάΕ | ‘Ιή÷–œ»≥ωœ÷Β≠ΜΤ…ΪΙΧΧεΘ§Κσ≥ωœ÷ΜΤ…ΪΙΧΧε | ‘Ιή÷–“ΚΧε±δΜκΉ««“»»Υ°÷– Ήœ»≥ωœ÷ΜκΉ« |
Ϋα¬έ | ΤδΥϊΧθΦΰ≤Μ±δ ±Θ§Ζ¥”ΠΈο≈®Ε»‘Ϋ¥σΘ§Ζ¥”ΠΥΌ¬ ‘ΫΩλ | ―θΜ·–‘ΘΚCl2>Br2>I2 | »ήΫβΕ»ΘΚAgCl>AgBr>AgI | ≤ΜΡήΥΒΟςΈ¬Ε»‘ΫΗΏΘ§ΥΌ¬ ‘ΫΩλ |
A.AB.BC.CD.D
ΓΨ¥πΑΗΓΩD
ΓΨΫβΈωΓΩ
A. ”ΠΗΟΑ―Ά§ΧεΜΐΓΔ≤ΜΆ§≈®Ε»ΒΡ≤ίΥα»ή“ΚΦ”»κΒΫœύΆ§ΧεΜΐΓΔœύΆ§≈®Ε»ΒΡKMnO4»ή“Κ÷–Θ§ΗυΨί»ή“ΚΆ …Ϊ ±ΦδΒΡ≥ΛΕΧ≈–Εœ≈®Ε»Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§ΗΟ Β―ι≤ΌΉςΥ≥–ρΒΏΒΙΘ§≤ΜΡήΙΜΒΟΒΫ’ΐ»ΖΫα¬έΘ§A¥μΈσΘΜ
B. Cl2”κNaBrΖΔ…ζ÷ΟΜΜΖ¥”Π≤ζ…ζBr2Θ§ ΙΉσ±ΏΟό«ρ±δΜΤΘ§Br2“ΉΜ”ΖΔΘ§Μα”κ”“±ΏΒΡΟό«ρ…œKIΖΔ…ζ÷ΟΜΜΖ¥”Π≤ζ…ζI2Θ§I2”ωΒμΖέ»ή“Κ±δάΕ…ΪΘ§”“±ΏΟό«ρ±δΈΣάΕ…Ϊ“≤”–Ω…Ρή «ΙΐΝΩΒΡΈ¥Ζ¥”ΠΒΡCl2”κKIΖΔ…ζ÷ΟΜΜΖ¥”Π≤ζ…ζΒΡI2Υυ÷¬Θ§“ρ¥Υ≤ΜΡή÷ΛΟς―θΜ·–‘ΘΚCl2>Br2>I2Θ§B¥μΈσΘΜ
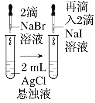
C. œρ2 mLΚ§”–AgCl–ϋΉ«“ΚΒΡ ‘Ιή÷–ΒΈΦ”2ΒΈNaBr»ή“ΚΘ§≤ζ…ζΒ≠ΜΤ…Ϊ≥ΝΒμΘ§Ω…÷ΛΟςΈο÷ ΒΡ»ήΫβΕ»AgCl>AgBrΘ§ΒΪ”…”ΎΤδ÷–AgCl–ϋΉ«“ΚΙΐΝΩΘ§“ρ¥Υ‘ΌœρΗΟΜλΚœΈο÷–ΒΈΦ”2ΒΈNaI»ή“Κ ±Θ§≤ζ…ζΜΤ…Ϊ≥ΝΒμΘ§÷ΜΡήΒΟΒΫΫα¬έΘΚ»ήΫβΕ»ΘΚAgCl>AgIΘ§Εχ≤ΜΡή÷ΛΟςΈο÷ ΒΡ»ήΫβΕ»AgBr>AgIΘ§C¥μΈσΘΜ
D. ΝΫ÷÷»ή“ΚΜλΚœ«ΑΈο÷ ΒΡ≈®Ε»œύΒ»Θ§ΧεΜΐ“≤œύΆ§Θ§ΜλΚœΚσΨΆ“―Ψ≠ΖΔ…ζΝΥΜ·―ßΖ¥”ΠΘ§»ΜΚσ‘ΌΖ÷±πΖ≈»κ≤ΜΆ§Έ¬Ε»ΒΡΥ°÷–“―Ψ≠Έό»ΈΚΈ“β“εΘ§≤ΜΡήΥΒΟςΈ¬Ε»‘ΫΗΏΘ§ΥΌ¬ ‘ΫΩλΓΘ”ΠΗΟΑ―2÷ß Δ”–5 mL 0.1 mol/LΒΡNa2S2O3»ή“ΚΒΡ ‘ΙήΚΆ2÷ß Δ”–5 mL 0.1 mo/LΒΡΝρΥα»ή“ΚΖ÷≥…ΝΫΉιΘ§“ΜΉιΖ≈»κ»»Υ°÷–Θ§“ΜΉιΖ≈»κάδΥ°÷–Θ§“ΜΕΈ ±ΦδΚσΜλΚœΟΩ“ΜΉιΒΡΝΫ÷÷Έο÷ ΒΡΥ°»ή“ΚΘ§ΗυΨίΖ¥”Π≥ωœ÷ΜκΉ«ΒΡΩλ¬ΐΘ§ά¥±»ΫœΈ¬Ε»Ε‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§D’ΐ»ΖΘΜ
Ι Κœάμ―Γœν «DΓΘ

 ―τΙβΩΈΧΟΆ§≤ΫΝΖœΑœΒΝ–¥πΑΗ
―τΙβΩΈΧΟΆ§≤ΫΝΖœΑœΒΝ–¥πΑΗ