题目内容
【题目】将a L NH3通入某恒压的密闭容器中,在一定条件下让其分解,达到平衡后气体体积增大到b L(气体体积在相同条件下测定)。下列说法中正确的是( )
A.平衡后氨气的分解率为![]()
B.平衡混合气体H2的体积分数为![]()
C.反应前后气体的密度比为![]()
D.平衡后气体的平均摩尔质量为![]()
【答案】B
【解析】
发生2NH3![]() N2+3H2,根据化学计量数的意义,以及差量法进行分析;
N2+3H2,根据化学计量数的意义,以及差量法进行分析;

A. 根据上述,消耗NH3的体积为(b-a)L,则氨气的分解率为![]() ,故A错误;
,故A错误;
B. 达到平衡,NH3的体积为[a-(b-a)]L=(2a-b)L,生成N2的体积为![]() L,生成H2的体积为
L,生成H2的体积为![]() L,则达到平衡时,H2的体积分数为
L,则达到平衡时,H2的体积分数为![]() =
=![]() ,故B正确;
,故B正确;
C. 组分都是气体,则混合气体总质量保持不变,根据![]() ,因此有反应前后气体的密度之比等于体积的反比,即反应前后气体的密度比为
,因此有反应前后气体的密度之比等于体积的反比,即反应前后气体的密度比为![]() ,故C错误;
,故C错误;
D. 相同条件下,气体体积之比等于物质的量之比,组分都是气体,气体质量保持不变,即为17a g,因此平衡后气体的平均摩尔质量为![]() =
=![]() g·mol-1,故D错误;
g·mol-1,故D错误;
答案:B。

【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
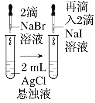
装置或操作 | 取两支试管各加入4 mL 0.01 mol/L的草酸溶液,分别滴加2 mL 0.1 mol/L、0.2 mol/L的高锰酸钾溶液 |
|
| 向分别盛有5 mL 0.1 mol/L的硫代硫酸钠溶液的试管中滴加5 mL 0.1 mo/L的硫酸溶液,一段时间后,分别放在冷水和热水中。 |
现象 | 褪色并观察褪色的时间 | 左边棉球变黄,右边棉球变蓝 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊且热水中首先出现浑浊 |
结论 | 其他条件不变时,反应物浓度越大,反应速率越快 | 氧化性:Cl2>Br2>I2 | 溶解度:AgCl>AgBr>AgI | 不能说明温度越高,速率越快 |
A.AB.BC.CD.D
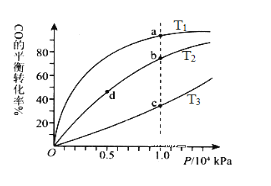
【题目】700℃时,H2(g)+CO2(g)![]() H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025 mol/(L·min),下列判断不正确的是()
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025 mol/(L·min),下列判断不正确的是()
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/mol/L | 0.1 | 0.2 | 0.2 |
C(CO2)/mol/L | 0.1 | 0.1 | 0.2 |
A. 平衡时,乙中CO2的转化率大于50%
B. 当反应平衡时,丙中c(CO2)是甲中的2倍
C. 温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应
D. 其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/L CO2,到达平衡时c (CO)与乙不同