题目内容
【题目】骨胶黏剂是一种极具应用前景的医用高分子材料。某骨胶黏剂的制备原料为聚酯三元醇,其合成原理如下:
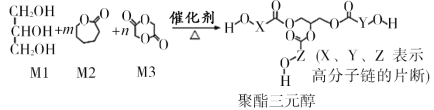
已知:R1COOR2+R318OH![]() R1CO18OR3+R2OH
R1CO18OR3+R2OH
下列说法正确的是
A.单体Ml可用于配制化妆品,且分子中含有3个手性碳原子
B.改变Ml在三种单体中的比例,可调控聚酯三元醇的相对分子质量
C.该合成反应为缩聚反应
D.X、Y、Z中包含的结构片段可能有![]()
【答案】BD
【解析】
A.单体Ml是丙三醇,俗称甘油,具有强的吸水性,可用于配制化妆品,分子中无手性碳原子,A错误;
B.改变M1在三种单体中的比例,则生成物不同,则改变M1在三种单体中的比例,可调控聚酯三元醇的相对分子质量,B正确;
C.如发生缩聚反应,应生成高分子化合物,而聚酯三元醇相对分子质量较小,因此发生的不是缩聚反应,C错误;
D.如涉及M2、M3之间的取代,则存在该片段,D正确;
故合理选项是BD。

【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置或操作 | 取两支试管各加入4 mL 0.01 mol/L的草酸溶液,分别滴加2 mL 0.1 mol/L、0.2 mol/L的高锰酸钾溶液 |
|
| 向分别盛有5 mL 0.1 mol/L的硫代硫酸钠溶液的试管中滴加5 mL 0.1 mo/L的硫酸溶液,一段时间后,分别放在冷水和热水中。 |
现象 | 褪色并观察褪色的时间 | 左边棉球变黄,右边棉球变蓝 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊且热水中首先出现浑浊 |
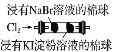
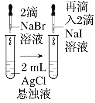
结论 | 其他条件不变时,反应物浓度越大,反应速率越快 | 氧化性:Cl2>Br2>I2 | 溶解度:AgCl>AgBr>AgI | 不能说明温度越高,速率越快 |
A.AB.BC.CD.D
【题目】下表是五种主族元素的结构特点及其元素、单质、化合物的性质.
元素 | 结构特点及元素、单质、化合物的性质 |
X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
W | 最外层电子排布(n+1)sn(n+1)pn﹣1 |
T | 单质升华可以产生紫色的烟 |
(1)写出X元素的原子核外电子排布__;其单质的化学性质__(填“稳定”或“活泼”),该元素的非金属性__(填“强”或“弱”),证明其强弱的理由是__.
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式__;已知w的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为__.
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:__,__.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为__.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.