题目内容
【题目】常温下,![]() 先将
先将![]() 溶于水制成
溶于水制成![]() 溶液,然后取出
溶液,然后取出![]() 溶液滴加
溶液滴加![]() 溶液,整个过程中利用
溶液,整个过程中利用![]() 数据采集器测得溶液的
数据采集器测得溶液的![]() 变化曲线如图所示(实验过程中不考虑
变化曲线如图所示(实验过程中不考虑![]() 的挥发和
的挥发和![]() 的分解)。下列说法正确的是
的分解)。下列说法正确的是
A.![]() 过程中,是氯气溶于水的过程,
过程中,是氯气溶于水的过程,![]() 和水的电离程度均不断增大
和水的电离程度均不断增大
B.![]() 点溶液中
点溶液中![]() 接近于
接近于![]()
C.![]() ,溶液中
,溶液中![]()
D.滴加![]() 溶液的体积为
溶液的体积为![]() 时,
时,![]()
【答案】C
【解析】
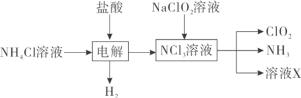
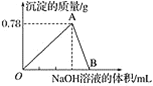
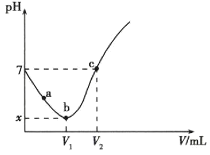
常温下,纯水的pH=7,题图曲线的起点为纯水,从起点至b点为将Cl2通入水中得到氯水的过程,此过程中发生反应Cl2+H2OH++Cl-+HClO;b点往后为向氯水中滴加NaOH溶液的过程,此过程中发生反应Cl2+2NaOH=NaCl+NaClO+H2O,100mL溶液中溶解了0.01mol×![]() =0.001mol,根据反应Cl2+2NaOH=NaCl+NaClO+H2O,Cl2与NaOH完全反应时消耗NaOH溶液的体积为0.002mol÷0.1mol/L=20mL,此时溶液中溶质为NaCl和NaClO,由于ClO-的水解溶液呈碱性。
=0.001mol,根据反应Cl2+2NaOH=NaCl+NaClO+H2O,Cl2与NaOH完全反应时消耗NaOH溶液的体积为0.002mol÷0.1mol/L=20mL,此时溶液中溶质为NaCl和NaClO,由于ClO-的水解溶液呈碱性。
A. Cl2与水的反应为Cl2+H2O![]() H++C1-+HClO,由题图可知a~b过程中,pH不断减小,c(H+)不断增大,酸性越强,对水的电离抑制程度增大,则水的电离程度不断减小,A错误;
H++C1-+HClO,由题图可知a~b过程中,pH不断减小,c(H+)不断增大,酸性越强,对水的电离抑制程度增大,则水的电离程度不断减小,A错误;
B.根据反应Cl2+H2OH++Cl-+HClO,若0.01molCl2溶于水时与水完全反应,则生成0.01molHCl和0.01molHClO,HCl完全电离、HClO部分电离,溶液中c(H+)略大于0.01mol/L,溶液的pH略小于2,c(HClO) ≈10-2mol/L,根据![]() 和c(H+)=10-xmol/L得出
和c(H+)=10-xmol/L得出![]() ,但0.0lmoCl2溶于水时只有部分Cl2与水反应,故溶液中c(H+)<0.01mol/L,溶液的pH>2,生成的n(HClO)<0.01mol,溶液中c(HClO)<0.01mol/L,故c(ClO-)比
,但0.0lmoCl2溶于水时只有部分Cl2与水反应,故溶液中c(H+)<0.01mol/L,溶液的pH>2,生成的n(HClO)<0.01mol,溶液中c(HClO)<0.01mol/L,故c(ClO-)比![]() 小,B错误;
小,B错误;
C. c点溶液pH=7,根据分析,c点加入的NaOH溶液的体积小于20mL,即V2-V1<20,此时溶液中的电荷守恒为c(Na+)+c(H+)=c(Cl-)+c(ClO-)+c(OH-),因c(H+)=c(OH-),则c(Na+)=c(Cl-)+c(ClO-),根据反应中的得失电子守恒和物料守恒,c(Cl-)=c(ClO-)+c(HClO),将两式整理得c(Na+)=2c(ClO-)+c(HClO),C正确;
D. 根据分析,加入NaOH溶液的体积为20mL时,Cl2与NaOH恰好完全反应,得到含等物质的量浓度的NaCl和NaClO的混合液,溶液中的物料守恒为c(Na+)=c(Cl-)+c(ClO-)+c(HClO),D错误;
答案选C。

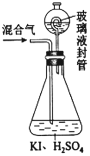
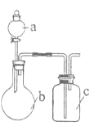
【题目】利用如图实验装置进行相关实验,能得出相应实验结论的是( )
a | b | c | 实验结论 |
| |
A | 浓醋酸 | CaCO3 | C6H5ONa溶液 | 酸性:碳酸>苯酚 | |
B | Br2的苯溶液 | 铁屑 | AgNO3溶液 | 苯和液溴发生取代反应 | |
C | 浓盐酸 | 酸性KMnO4溶液 | 碘化钾溶液 | 氧化性:Cl2>I2 | |
D | 饱和食盐水 | 电石 | 酸性KMnO4溶液 | 乙炔具有还原性 |
A.AB.BC.CD.D
【题目】实验室制备纯碱的主要步骤如流程所示:

四种盐在不同温度下的溶解度(g/100gH2O)表
温度 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
提示:温度高于35℃时NH4HCO3会分解,请回答:
(1)下列操作或描述正确的是________。
A.温度控制在30-35℃是因为温度太高NH4HCO3会分解,温度太低反应速率太慢
B.保温30min的目的是使反应充分进行
C.过滤后的滤液只有NH4Cl和NH4HCO3溶质
D.洗去晶体表面的杂质可以选用蒸馏水
(2)反应温度控制在30~35℃,为控制此温度范围,采取的加热方法为______________。
(3)常温时,过滤后主要得到NaHCO3晶体的原因是______________。
(4)灼烧NaHCO3晶体的装置为________。
A.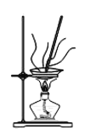 B.
B.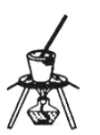 C.
C.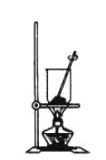
(5)洗涤NaHCO3晶体的操作______________。
(6)测定纯碱产品中NaHCO3含量的方法:准确称取纯碱样品Wg放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用物质的量浓度为c(mol·L-1)的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点)所用HCl溶液体积为V1mL。再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HCl溶液体积为V2mL,写出纯碱样品中NaHCO3质量分数的计算式:______________。