题目内容
【题目】已知CuO高温灼烧生成Cu2O,Cu2O与稀H2SO4反应的离子方程式为:Cu2O+2H+═Cu+Cu2++H2O。现将经高温灼烧后的CuO样品投入足量稀硫酸中得到混合溶液,有关说法正确的是( )
A.反应中Cu2O只作氧化剂
B.若有28.8g Cu2O参加反应,则转移电子数为0.2NA
C.Cu2O的稳定性比CuO弱
D.如果溶液中出现蓝色,说明CuO已分解
【答案】B
【解析】
A、根据反应中Cu元素的化合价变化判断;
B、根据n=![]() 计算出28.8g Cu2O物质的量,反应Cu2O+2H+═Cu+Cu2++H2O中,1mol氧化亚铜完全反应注意1mol电子,据此计算转移电子的物质的量及数目;
计算出28.8g Cu2O物质的量,反应Cu2O+2H+═Cu+Cu2++H2O中,1mol氧化亚铜完全反应注意1mol电子,据此计算转移电子的物质的量及数目;
C、高温下氧化亚铜被氧化铜温度;
D、CuO与稀硫酸反应生成硫酸铜,溶液呈蓝色。
A、反应Cu2O+2H+═Cu+Cu2++H2O中Cu元素的化合价从+1价升高+2价,部分降低到0价,则Cu2O既是氧化剂又是还原剂,故A错误;
B、反应Cu2O+2H+═Cu+Cu2++H2O中,1mol氧化亚铜完全反应注意1mol电子,28.8g Cu2O物质的量为:![]() =0.2mol,0.2mol氧化亚铜完全反应转移了0.2mol电子,转移电子数为0.2NA,故B正确;
=0.2mol,0.2mol氧化亚铜完全反应转移了0.2mol电子,转移电子数为0.2NA,故B正确;
C、二者稳定性需要根据所处条件分析,在温度不是很高时CuO比氧化亚铜稳定,在高温的时候,氧化亚铜比氧化铜稳定,故C错误;
D、如果溶液中出现蓝色,不能说明CuO已分解,因为CuO与稀硫酸反应溶液也呈蓝色,故D错误;
答案选B。

【题目】甲苯(![]() )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(![]() )、苯甲酸(
)、苯甲酸(![]() )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度(ρ水=1g·cm-3) | 溶解性 | |
水 | 乙醇 | |||||
甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。
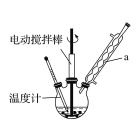
(1)装置a的名称是______________,为使反应体系受热比较均匀,可________。
(2)三颈瓶中发生反应的化学方程式为_______________________________________________________。
(3)写出苯甲醛与银氨溶液在一定的条件下发生反应的化学方程式:________________________________。
(4)反应完毕后,反应混合液经过自然冷却至室温时,还应经过___________、__________(填操作名称)等操作,才能得到苯甲醛粗产品。
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸。若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是______________(按步骤顺序填字母)。
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.加入适量碳酸氢钠溶液混合振荡