题目内容
16.如图所示的电化学装置,电解质溶液为Na2SO4,下列说法不正确的是( )
| A. | 当闭合开关S1,断开开关S2,右石墨棒发生的电极反应为:2H2O-4e-=4H++O2↑ | |
| B. | 石墨棒使用前在高温火焰上灼烧至红热,迅速浸入冷水,可以使表面粗糙多空,吸附更多的气体 | |
| C. | 先闭合开关S1,一段时间后断开,再闭合S2,可以观察到发光二级管发光 | |
| D. | 断开S2,闭合S1,更换电解质,可以用来模拟工业制氯气,粗铜冶炼制精铜 |
分析 由发光二极管可知左侧电极为负极,右侧电极为正极,则闭合开关S1,断开开关S2时,为电解池装置,电解硫酸钠溶液,左侧应生成氢气,则为阴极,右侧生成氧气,为阳极,以此解答该题.
解答 解:由发光二极管可知左侧电极为负极,右侧电极为正极,则闭合开关S1,断开开关S2时,为电解池装置,电解硫酸钠溶液,左侧应生成氢气,则为阴极,右侧生成氧气,为阳极,
A.当闭合开关S1,断开开关S2,右石墨棒为阳极,发生氧化反应生成氧气,电极方程式为2H2O-4e-=4H++O2↑,故A正确;
B.高温条件下,碳和水反应生成CO和氢气,可使碳表面粗糙多空,吸附更多的气体,故B正确;
C.先闭合开关S1,一段时间后断开,再闭合S2,电极两侧分别有氢气、氧气,形成原电池反应,可以观察到发光二级管发光,故C正确;
D.粗铜冶炼制精铜,阳极材料为粗铜,如电极材料不变,则不能精炼铜,故D错误.
故选D.
点评 本题综合考查原电池、电解池知识,为高频考点,侧重于学生的分析能力的考查,注意把握电解池、原电池工作原理,把握电解方程式的书写,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列说法中错误的是( )
| A. | Al2(SO4)3可除去酸性废水中的悬浮颗粒 | |
| B. | 医药中常用酒精来消毒,是因为酒精能够使细菌蛋白发生变性 | |
| C. | 煤通过气化、液化和干馏等可获得清洁能源和重要的化工原料 | |
| D. | 高锰酸钾溶液和双氧水进行环境消毒时原理相同 |
12.下列说法正确的是( )
| A. | 分子式为C5H12的同分异构体中,一氯代物仅有一种的有机物一定是2,2一二甲基戊烷. | |
| B. | 若某高分子化合物对应的单体有两种,则此高聚物一定是通过缩聚反应得到的. | |
| C. | 等物质的量的乙烯和乙醇在足量氧气中完全燃烧,消耗O2和生成CO2的量相等 | |
| D. | 苯丙氨酸的结构为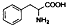 ,分子式为C9H10NO2,它既能与酸反应又能与碱反应. ,分子式为C9H10NO2,它既能与酸反应又能与碱反应. |
1.表是元素周期表的一部分,Y原子最外层电子数是次外层电子数的3倍,下列说法正确的是( )
| X | Y | ||
| M | Z |
| A. | 简单氢化物稳定性:X>Z | B. | 简单离子半径:Y<M | ||
| C. | 最高价氧化物水化物的酸性:Z<M | D. | 得电子能力:X>Y |
6.下列说法不正确的是( )
| A. | 在船外壳镶嵌锌块保护船身,锌为原电池的负极 | |
| B. | MgO的熔点高于NaCl,是因为MgO的晶格能大于NaCl | |
| C. | 1molFeCl3完全水解将产生6.02×1023个胶体粒子 | |
| D. | 水的离子积常数Ksp随着温度的升高而增大,说明水的电离是吸热过程 |
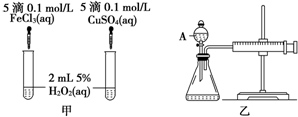 (1)下列反应属于吸热反应的是DE
(1)下列反应属于吸热反应的是DE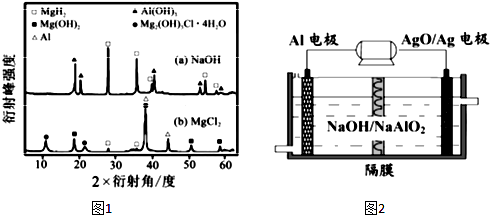
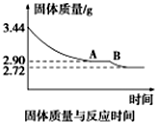 煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题: