题目内容
下列说法正确的是( )
| A、常温常压下,8克O3含有0.5NA个氧原子(相对原子质量O:16) |
| B、1mol?L-1的Ca(ClO)2溶液中含ClO-数目为2NA |
| C、标准状况下,22.4L HCl溶于1L水中所得的盐酸含有NA个HCl分子 |
| D、1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.臭氧中只含有氧原子,8个臭氧中含有8g氧原子,含有0.5mol氧原子;
B.缺少次氯酸钙溶液的体积,无法计算溶液中次氯酸根离子的数目;
C.氯化氢溶于1L水中,所得溶液的体积不是1L;
D.钠为1价金属,1mol钠完全反应失去1mol电子.
B.缺少次氯酸钙溶液的体积,无法计算溶液中次氯酸根离子的数目;
C.氯化氢溶于1L水中,所得溶液的体积不是1L;
D.钠为1价金属,1mol钠完全反应失去1mol电子.
解答:
解:A.8g臭氧中含有8g O原子,含有氧原子的物质的量为0.5mol,含有0.5NA个氧原子,故A正确;
B.没有告诉次氯酸钙溶液的体积,无法计算溶液中次氯酸根离子的数目,故B错误;
C.标准状况下,22.4L氯化氢的物质的量为1mol,1mol氯化氢溶于1L水中,所得溶液的体积不是1L,溶液的浓度不是1mol/L,故C错误;
D.1mol钠完全反应失去1mol电子,失去NA个电子,故D错误;
故选A.
B.没有告诉次氯酸钙溶液的体积,无法计算溶液中次氯酸根离子的数目,故B错误;
C.标准状况下,22.4L氯化氢的物质的量为1mol,1mol氯化氢溶于1L水中,所得溶液的体积不是1L,溶液的浓度不是1mol/L,故C错误;
D.1mol钠完全反应失去1mol电子,失去NA个电子,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意题中缺少溶液体积,且次氯酸根离子部分水解.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
能与氢氧化钠溶液反应且属化合物的原子晶体是( )
| A、铝 | B、金刚石 | C、硅 | D、二氧化硅 |
下列化学用语正确的是( )
| A、乙烯的结构简式:CH2CH2 |
| B、葡萄糖的结构式:C6H12O6 |
C、顺-2-丁烯的结构简式: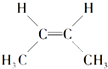 |
| D、乙酸的实验式:C2H4O2 |
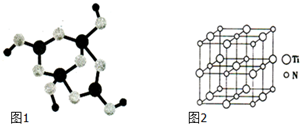
仔细观察图.这种堆积方式是( )
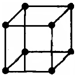

| A、钾型 | B、简单立方 |
| C、镁型 | D、铜型 |
铅蓄电池在人们的日常生活中的应用很广泛.构成铅蓄电池的两极分别为Pb、PbO2,电解质为硫酸溶液,反应方程式为Pb+PbO2+2H2SO4
2PbSO4+2H2O.以下说法中不正确的是( )
| 放电 |
| 充电 |
| A、放电时,Pb为负极,被氧化 |
| B、充电时,PbO2为阴极,被还原 |
| C、充电时,溶液的pH不断减小 |
| D、若放电过程中转移了0.4mol电子,则消耗Pb的质量为41.4g |