题目内容
向2份0.1mol?L-1 CH3COONa溶液中分别加入少量NH4NO3、Na2SO3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为 、 (填“减小”、“增大”或“不变”)
考点:影响盐类水解程度的主要因素
专题:盐类的水解专题
分析:有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.
解答:
解:CH3COONa是强碱弱酸盐其水溶液呈碱性,NH4NO3是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加硝酸铵会促进醋酸根离子水解,导致醋酸根离子浓度减小;
Na2SO3是强碱弱酸盐其水溶液呈碱性,所以向醋酸钠溶液中加亚硫酸钠会抑制醋酸根离子的水解,导致醋酸根离子浓度增大;
故答案为:减小;增大.
Na2SO3是强碱弱酸盐其水溶液呈碱性,所以向醋酸钠溶液中加亚硫酸钠会抑制醋酸根离子的水解,导致醋酸根离子浓度增大;
故答案为:减小;增大.
点评:本题考查了影响盐类水解的因素,明确含有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列说法正确的是( )
| A、常温常压下,8克O3含有0.5NA个氧原子(相对原子质量O:16) |
| B、1mol?L-1的Ca(ClO)2溶液中含ClO-数目为2NA |
| C、标准状况下,22.4L HCl溶于1L水中所得的盐酸含有NA个HCl分子 |
| D、1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
下列指定粒子的个数比为1:1的是( )
| A、NH4+中质子数与电子数 |
| B、OH-中电子数与中子数 |
| C、Na2O2中阳离子与阴离子 |
| D、NH4HSO4晶体中阳离子与阴离子 |
下列化学方程式正确的是( )
| A、CH3COONa+CO2+H2O→CH3COOH+NaHCO3 |
B、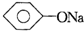 +CO2+H2O→ +CO2+H2O→ +NaHCO3 +NaHCO3 |
C、2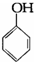 +3Br2→ +3Br2→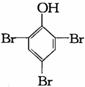 ↓ ↓ |
D、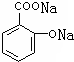 +2CO2+2H2O→ +2CO2+2H2O→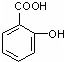 +2NaHCO3 +2NaHCO3 |
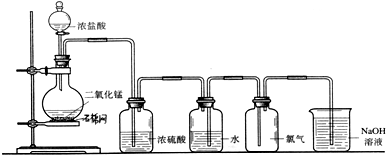
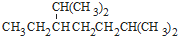 的名称为
的名称为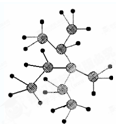 名称
名称 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题: