题目内容
能与氢氧化钠溶液反应且属化合物的原子晶体是( )
| A、铝 | B、金刚石 | C、硅 | D、二氧化硅 |
考点:原子晶体
专题:化学键与晶体结构
分析:常见的原子晶体有:一些非金属单质,如金刚石、硼、硅、锗等;一些非金属化合物,如二氧化硅、碳化硅、氮化硼等,化合物由两种或两种以上的元素组成的纯净物.再结合物质的性质判断.
解答:
解:A、铝属于金属晶体,能与氢氧化钠溶液反应,是单质不是化合物,故A错误;
B、金刚石属于原子晶体,不能与氢氧化钠溶液反应,是单质不是化合物,故B错误;
C、硅属于原子晶体,能与氢氧化钠溶液反应,是单质不是化合物,故C错误;
D、二氧化硅属于原子晶体,能与氢氧化钠溶液反应,是化合物,故D正确;
故选D.
B、金刚石属于原子晶体,不能与氢氧化钠溶液反应,是单质不是化合物,故B错误;
C、硅属于原子晶体,能与氢氧化钠溶液反应,是单质不是化合物,故C错误;
D、二氧化硅属于原子晶体,能与氢氧化钠溶液反应,是化合物,故D正确;
故选D.
点评:本题考查常见物质晶体类型判断、物质性质等,难度不大,掌握常见物质晶体类型及常见原子晶体即可解答.

练习册系列答案
相关题目
下列说法正确的是( )
| A、常温常压下,8克O3含有0.5NA个氧原子(相对原子质量O:16) |
| B、1mol?L-1的Ca(ClO)2溶液中含ClO-数目为2NA |
| C、标准状况下,22.4L HCl溶于1L水中所得的盐酸含有NA个HCl分子 |
| D、1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
下列各组元素原子中,按金属性依次增强或非金属性依次减弱的是( )
| A、Na,Mg,Al |
| B、N,O,F |
| C、Li,Na,K |
| D、Cl,I,Br |
下列指定粒子的个数比为1:1的是( )
| A、NH4+中质子数与电子数 |
| B、OH-中电子数与中子数 |
| C、Na2O2中阳离子与阴离子 |
| D、NH4HSO4晶体中阳离子与阴离子 |
某种有机物如图所示,有关该物质的说法正确的是( )
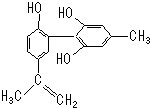

| A、由于酚酸性比碳酸弱,故此物质不可能与碳酸钠溶液反应 |
| B、滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、1mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4mol、7mol |
| D、该分子中的所有原子可能共平面 |
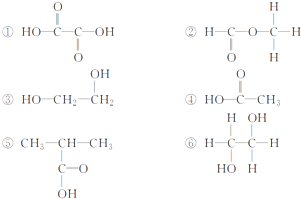
 、CH3CH2OH中与甲烷互为同系物的是
、CH3CH2OH中与甲烷互为同系物的是