题目内容
18. 一定条件下,在2L密闭容器中加入等物质的量的FeO和CO,发生下列反应FeO(s)+CO(g)═Fe(s)+CO2(g),在T1、T2温度下,物质的量n随时间t变化的曲线如图所示,下列叙述正确的是( )
一定条件下,在2L密闭容器中加入等物质的量的FeO和CO,发生下列反应FeO(s)+CO(g)═Fe(s)+CO2(g),在T1、T2温度下,物质的量n随时间t变化的曲线如图所示,下列叙述正确的是( )| A. | 平衡前,随着反应的进行,容器内气体的相对分子质量始终不变 | |
| B. | 平衡时,其他条件不变,取出适当铁可提高CO的转化率 | |
| C. | 该反应的△H<0,K1<K2=1.5 | |
| D. | 当反应进行到t1时刻仅改变一个条件,可能是通入了氮气 |
分析 结合图可知,温度为T1先到达平衡,所以T1>T2,T1时消耗FeO为2.0-1.0=1.0mol,所以生成二氧化碳为1.0mol,又T2时生成二氧化碳为1.2mol,所以升温平衡向逆反应方向移动;
A.平衡前,随着反应的进行,气体又CO变成二氧化碳,所以容器内气体的相对分子质量一直增大;
B.改变纯固体平衡不移动;
C.根据以上分析,升温平衡向逆反应方向移动,该反应为放热反应,温度高平衡常数越小;
D.在2L密闭容器中加入不反应的气体,平衡不移动;
解答 解:结合图可知,温度为T1先到达平衡,所以T1>T2,T1时消耗FeO为2.0-1.0=1.0mol,所以生成二氧化碳为1.0mol,又T2时生成二氧化碳为1.2mol,所以升温平衡向逆反应方向移动;
A.平衡前,随着反应的进行,气体又CO变成二氧化碳,所以容器内气体的相对分子质量一直增大,故A错误;
B.因为铁为纯固体,所以取出适当铁,平衡不移动,CO的转化率不变,故B错误;
C.根据以上分析,升温平衡向逆反应方向移动,该反应为放热反应,温度高平衡常数越小,即△H<0,K1<K2=$\frac{1.2}{2.0-1.2}$=1.5,故C正确;
D.在2L密闭容器中加入不反应的氮气气体,平衡不移动,故D错误;
故选C.
点评 本题考查了化学平衡中浓度随时间变化的曲线分析,涉及了外界条件对平衡移动影响等知识,题目难度中等,根据图象判断反应为放热反应是解题的关键,注意把握图象中曲线的变化特点,明确外界条件对化学平衡的影响.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.请根据题意,选择恰当的选项用字母代号填空.
(1)根据如表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填人对应“答案”的空格中.
(2)现有:A.铁锅;B、鸡蛋;C、白酒;D、乙烯.根据所学知识,请你在上述四种物质中选择合适的物质填入下列空格中(填编号)
①可以作为水果催熟剂的是D; ②富含乙醇的是C;
③在潮湿的空气中会生锈的是A; ④富含蛋白质的是B.
(3)青霉素是最重要的抗生素.青霉素在人体内经酸性水解后,得到青霉素氨基酸,其结构简式如图所示:
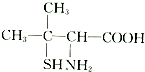
青霉素氨基酸中含有的官能团的名称为氨基、羧基.
(1)根据如表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填人对应“答案”的空格中.
| 实验操作 | 答案 | 实验现象 |
| ①向鸡蛋清溶液里加入饱和硫酸铵溶液 | A.呈蓝色 B.呈黄色 C、析出白色沉淀 D.出现光亮的银镜 | |
| ②向银氨溶液中加人葡萄糖溶液后水浴加热 | ||
| ③向鸡蛋清溶液里滴加浓硝酸后微热 | ||
| ④向士豆片上滴加碘水 |
①可以作为水果催熟剂的是D; ②富含乙醇的是C;
③在潮湿的空气中会生锈的是A; ④富含蛋白质的是B.
(3)青霉素是最重要的抗生素.青霉素在人体内经酸性水解后,得到青霉素氨基酸,其结构简式如图所示:

青霉素氨基酸中含有的官能团的名称为氨基、羧基.
6.日常生活中常用到化学知识,下列说法不正确的是( )
| A. | 赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 | |
| B. | 聚氯乙烯塑料有毒,不可用于制食品包装袋 | |
| C. | 明矾溶于水生成的Al (OH)3胶体,可除去水中的悬浮颗粒等杂质 | |
| D. | 新制的Cu(OH)2可以测定糖尿病患者尿中萄葡糖的含量 |
13.某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1mol•L-1,某同学进行了如下实验:
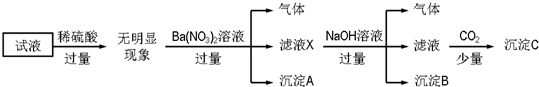
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 沉淀A是BaSO4,说明原试液中一定含有SO42- | |
| B. | 滤液X中大量存在的阳离子有NH4+、Fe3+和Ba2+ | |
| C. | 沉淀C只有一种成分 | |
| D. | 原溶液中一定大量存在的离子只有:NH4+、Fe2+、Cl-、SO42- |
3.下列关于有机化合物的说法正确的是( )
| A. | 乙酸和乙酸乙酯可用Na2CO3溶液加以区别 | |
| B. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| C. | 蛋白质和油脂都属于高分子化合物,一定条件下能水解 | |
| D. | 煤油可由煤干馏获得,可用作燃料和保存少量金属钠 |
10.常温下,下列离子浓度关系或结论正确的是( )
| A. | 将0.1mol/L氨水与0.1 mol/L稀盐酸等体积混合:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | 将pH=2 的稀盐酸与pH=12的氨水等体积混合,所得溶液pH>7 | |
| C. | 0.10 mol•L-1的氨水用HNO3溶液完全中和后,溶液显中性 | |
| D. | 用惰性电极电解稀硫酸时,实质是电解水,溶液的pH不变 |
7.用下列实验装置进行相应实验,能达到实验目的是( )
| A. | 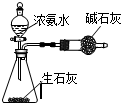 此图:制少量干燥的NH3 | |
| B. | 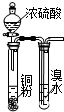 此图:验证浓硫酸具有强氧化性 | |
| C. | 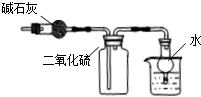 此图:干燥、收集并吸收多余SO2 | |
| D. | 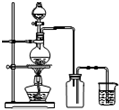 此图:实验室用MnO2和浓盐酸制取Cl2 |
 碳、氢、氧 3 种元素组成的有机物A,相对分子质量为 102,含氢的质量分数为9.8%,分子中氢原子个数为氧的 5 倍.
碳、氢、氧 3 种元素组成的有机物A,相对分子质量为 102,含氢的质量分数为9.8%,分子中氢原子个数为氧的 5 倍. 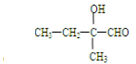 .
.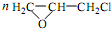 +CH2Cl+nOHCH2CH2OH$\stackrel{一定条件}{→}$
+CH2Cl+nOHCH2CH2OH$\stackrel{一定条件}{→}$ +nHCl
+nHCl