题目内容
13.下列各组离子在指定溶液中能大量共存的是( )| A. | 无色溶液:K-、Na+、Cu2+、OH- | |
| B. | 由水电离出的c(OH-)=10-13mol/L的溶液中:Na+、Ba2+、Cl-、Br+- | |
| C. | 加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ | |
| D. | 有较多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3- |
分析 A.无色溶液不含有色离子,离子之间不反应的能大量共存;
B.由水电离出的c(OH-)=10-13mol/L的溶液呈酸性或碱性;
C.加入Al能放出氢气的溶液为弱氧化性酸溶液或强碱溶液;
D.能和铁离子反应是离子不能大量共存.
解答 解:A.无色溶液中不含铜离子,且Cu2+、OH-生成沉淀,所以不能大量共存,故A错误;
B.由水电离出的c(H+)=1×10-14mol•L-1的溶液为酸性或者碱性溶液,这几种离子之间不反应且和氢离子或氢氧根离子都不反应,所以能大量共存,故B正确;
C.加入Al能放出H2的溶液中存在大量氢离子或氢氧根离子,HCO3-与氢离子、氢氧根离子反应,NH4+与氢氧根离子反应,在溶液中一定不能大量共存,故C错误;
D.Fe3+与SCN-反应生成络合物硫氰化铁,且碳酸氢根离子和铁离子发生双水解反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还要明确题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
3.在恒温恒容条件下,向容积为2L的密闭容器中充人2mol SO2和2mol O2,已知:2SO2(g)+O2(g)?2SO2(g);△H=-akJ/mol(a>0),经2min达到平衡状态,反应放热0.25a kJ.下列判断正确的是( )
| A. | 在1 min时:c(SO3)+c(SO2)=1.0mol/L | |
| B. | 2 min 内:v(SO2)=0.25mol/(L•min) | |
| C. | 若再充入2mol SO3,达平衡时SO3%(质量分数)减小 | |
| D. | 反应条件相同,若起始时向反应容器中充入2mol SO3,平衡时反应吸热0.75a kJ |
1.下列说法中错误的是( )
| A. | SO2、SO3都是极性分子 | |
| B. | 在H3O+和[Cu(H2O)4]2+中都存在配位键 | |
| C. | 元素电负性越大的原子,该元素的原子吸引键合电子的能力越强 | |
| D. | 原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
8.下列说法错误的是( )
| A. | 石油和天然气的主要成分都是碳氢化合物 | |
| B. | 乙醇、乙酸和乙酸乙酯可以用饱和碳酸钠溶液鉴别 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 甘氨酸(NH2-CH2-COOH)既能与NaOH反应,又能与盐酸反应 |
18.下列关于有机物的说法中,正确的是( )
| A. | 用水不能鉴别苯和溴苯 | |
| B. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| C. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| D. | 某有机物的分子结构如图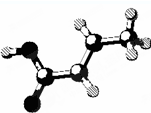 (图中棍表示单键、双键或叁键),它属于烃的含氧衍生物,该有机物可发生取代反应和加成反应 (图中棍表示单键、双键或叁键),它属于烃的含氧衍生物,该有机物可发生取代反应和加成反应 |
5.常温下,下列溶液中微粒浓度关系一定正确的是( )
| A. | 氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) | |
| B. | pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) | |
| C. | 0.1 mol•L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| D. | 0.1 mol•L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
2.下列各组中互为同位素的是( )
| A. | ${\;}_{19}^{40}$K与${\;}_{20}^{40}$Ca | B. | 正丁烷与异丁烷 | ||
| C. | ${\;}_{19}^{40}$K与${\;}_{19}^{39}$K | D. | 金刚石与石墨 |
3.下列有关化学用语正确的是( )
| A. | O原子的电子排布图为 | |
| B. | 氯化钠的分子式:NaCl | |
| C. | Cl-的结构示意图: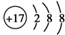 | |
| D. | Ca原子的电子排布式为 1s22s22p63s23p63d2 |
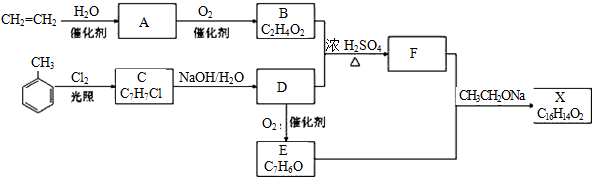
 .
. .
.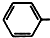 CH2OCH2CH2CHO
CH2OCH2CH2CHO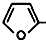 CH=CHCH2CH2CHO
CH=CHCH2CH2CHO COOCH2CH2CH3.
COOCH2CH2CH3.