题目内容
3.在一个5L的密闭容器中发生如下反应:3A(g)+B(g)→2C(g)+D(g),若最初加入的A和B都是5mol,在前10min内A的平均反应速率为0.10mol/(L•min ),则10min时,容器内B的物质的量是$\frac{10}{3}$mol.分析 根据速率之比等于化学计量数之比计算v(B),再根据v=$\frac{△c}{△t}$进行公式变形计算△c(B),根据△n=△c×V计算B的物质的量变化量,B的起始物质的量减去物质的量变化量即为计算10min时B的物质的量.
解答 解:速率之比等于化学计量数之比,故v(B)=$\frac{1}{3}$v(A)=$\frac{1}{3}$×0.10mol/(L•min ),
故△n=△c×V=)=$\frac{1}{3}$×0.10mol/(L•min )×10min×5L=$\frac{5}{3}$mol,
故10min时B的物质的量为5mol-$\frac{5}{3}$mol=$\frac{10}{3}$mol,
故答案为:$\frac{10}{3}$mol.
点评 本题考查化学反应速率有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.有八种物质:①甲烷 ②苯 ③聚乙烯 ④乙烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯 ⑧环己烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ③⑤⑧ | B. | ④⑤⑦ | C. | ④⑤⑧ | D. | ⑤⑦⑧ |
14.下列说法正确的是( )
| A. | H、D、T表示三种氢原子 | |
| B. | 卤族元素最高化合价均为正7价,最低化合价均为负1价 | |
| C. | 金属元素的原子最外层电子数,都少于4个 | |
| D. | 目前人们已发现了5000多种核素,说明发现了5000多种元素 |
18.下列有关晶胞的叙述正确的是( )
| A. | 晶胞是晶体中最小的结构基本单元 | |
| B. | 不同的晶体中晶胞的大小和形状都相同 | |
| C. | 晶胞中的任何一个粒子都完全属于该晶胞 | |
| D. | 晶胞都是正方体 |
8.下列实验方案可行的是( )
| A. | 用向下排空气法收集CO2 | B. | 用碱石灰干燥SO2 | ||
| C. | 通入Cl2出去FeCl3中FeCl2 | D. | 用HCl除去Na2CO3中的NaHCO3 |
2.下列各组物质中属于同分异构体的是( )
| A. | 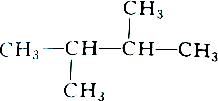 和 和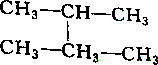 | B. | 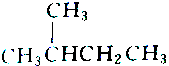 和 和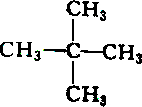 | ||
| C. | 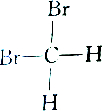 和 和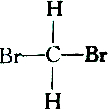 | D. | 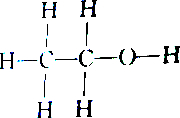 和 和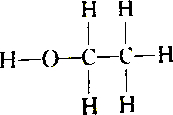 |
19.下列各组物质不互为等电子体的是( )
| A. | CO和N2 | B. | CO2和N2O | C. | CO32-和NO3- | D. | CO2和SO2 |
20.一定量的锌片与过量2mol•L-1的盐酸跟反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A. | 通入一定量的HCl气体 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入一定量6mol•L-1的硝酸溶液 | D. | 加入适量的CH3COONa固体 |