题目内容
15.一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ,经测定完全吸收生成的二氧化碳需消耗5mol/L的KOH溶液200mL,恰好生成正盐.则此条件下反应:C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(g)的△H为( )| A. | -16Q kJ/mol | B. | +8Q kJ/mol | C. | +16 Q kJ/mol | D. | -8 Q kJ/mol |
分析 充分燃烧一定量的丁烷发生的反应为:2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O,CO2恰好与KOH溶液完全反应生成正盐为K2CO3,2KOH+CO2═K2CO3+H2O,根据n=c×V计算KOH的物质的量,根据钾元素守恒计算n(K2CO3),根据碳元素守恒有n(CO2)=n(K2CO3),据此计算判断.
解答 解:KOH的物质的量为n(KOH)=c×V=0.2L×5mol/L=1mol,
2KOH+CO2═K2CO3+H2O,
根据钾离子守恒,故n(K2CO3)=mol×$\frac{1}{2}$=0.5mol,
根据碳元素守恒由n(CO2)=n(K2CO3)=0.5mol,
2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O
根据碳元素守恒可知,丁烷的物质的量为n(C4H10)=0.5mol×$\frac{1}{4}$=$\frac{1}{8}$mol,
即$\frac{1}{8}$mol丁烷放出的热量大小为QkJ,
故1mol丁烷完全燃烧放出的热量为QkJ×8=8QkJ,
则此条件下反应热化学方程式为C4H10(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(l)△H=-8Q kJ•mol-1,
故选D.
点评 本题考查反应热的计算,根据氢氧化钾确定丁烷的物质的量是解答该题的关键,题目难度中等.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
5.如图,下列装置能产生有效电流的是( )
| A. | 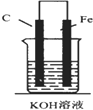 | B. | 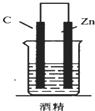 | C. | 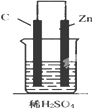 | D. |  |
6.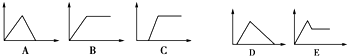 在图中,横坐标为向一定量的某溶液中加入某物质的量,纵坐标为生成沉淀的量.从图A~E中,选择适合表中各题要求的序号填入表中.
在图中,横坐标为向一定量的某溶液中加入某物质的量,纵坐标为生成沉淀的量.从图A~E中,选择适合表中各题要求的序号填入表中.
 在图中,横坐标为向一定量的某溶液中加入某物质的量,纵坐标为生成沉淀的量.从图A~E中,选择适合表中各题要求的序号填入表中.
在图中,横坐标为向一定量的某溶液中加入某物质的量,纵坐标为生成沉淀的量.从图A~E中,选择适合表中各题要求的序号填入表中.| 溶液 | 加(通)入物质 | 序号 |
| (1)饱和石灰水 | 通入过量CO2 | |
| (2)AlCl3溶液 | 加入过量的NH3•H2O | |
| (3)含少量NaOH的Na[Al(OH)4]溶液 | 通入过量CO2 | |
| (4)含少量NaOH的Na[Al(OH)4]溶液 | 逐滴加入稀盐酸 | |
| (5)MgCl2、AlCl3混合液 | 逐滴加入NaOH溶液至过量 | |
| (6)NaOH溶液 | 逐滴加入AlCl3溶液至过量 |
10.将pH=2的盐酸与pH=12的氨水等体积混合,在所得的混合溶液中,下列关系式正确的是( )
| A. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) | B. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | ||
| C. | c(Cl-)=c(NH4+)>c(H+)=c(OH-) | D. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
20.在pH=a的某电解质溶液中插入两支惰性电极,电解一段时间后,溶液pH<a,则电解质是( )
| A. | Na2SO4 | B. | KCl | C. | NaOH | D. | CuSO4 |
7.在1 000K时,已知反应Ni(s)+H2O(g)?NiO(s)+H2(g)的平衡常数K=2.当水蒸气和氢气的物质的量浓度相等时,此反应( )
| A. | 已达平衡状 | B. | 未达平衡状态,反应正向进行 | ||
| C. | 未达平衡状态,反应逆向进行 | D. | 无法确定 |
5.a、b、c、d是原子序数依次递增的四种元素,a、b、c三种元素的原子核外电子数之和与Cl-的核外电子数相等,a、c分别得到一个电子后均形成稀有气体原子的稳定电子层结构,d是生活中用量最大的金属,其简单离子有两种常见价态,下列说法正确的是( )
| A. | 离子半径:c>b>a | |
| B. | a与c形成化合物的溶液有毒,要密封保存于玻璃瓶中 | |
| C. | a2b2与d的一种较高价态离子的盐溶液混合时会产生大量的b2 | |
| D. | d高价离子在溶液中与c的低价离子因发生氧化还原反应而不能大量共存 |