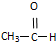题目内容
5.如图,下列装置能产生有效电流的是( )| A. | 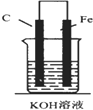 | B. | 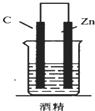 | C. | 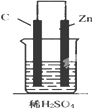 | D. |  |
分析 能产生有效电流即形成原电池,根据形成原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,据此分析解答.
解答 解:A.电解质为KOH溶液,不能自发的进行氧化还原反应,所以不能形成原电池,不能产生有效电流,故A错误;
B.电解质为酒精,不能自发的进行氧化还原反应,所以不能构成原电池,不能产生有效电流,故B错误;
C.电解质为H2SO4溶液,符合原电池的构成条件,所以能构成原电池,能产生有效电流,故C正确;
D.电解质为硫酸铜溶液,但该装置只有一个电极,所以不能构成原电池,不能产生有效电流,故D错误;
故选C.
点评 本题考查了原电池原理,明确原电池构成条件是解本题关键,根据原电池构成条件分析解答即可,这几个条件必须同时具备,缺一不可,题目难度不大.

练习册系列答案
相关题目
16.如图是某有机物分子的简易球棍模型.下列关于该有机物的说法中错误的是( )


| A. | 分子式为C3H7O2N | |
| B. | 该有机物能发生缩聚反应 | |
| C. | 能通过聚合反应生成高分子化合物 | |
| D. | 具有相同官能团的该有机物的同分异构体还有两种 |
13.已知化合物NH5的结构和NH4Cl相似,下列关于NH5的下列说法中正确的是( )
| A. | NH5是共价化合物 | |
| B. | NH5的电子式为NH4+[:H]- | |
| C. | NH5中氢元素呈价+1和-1价 | |
| D. | NH5与水发生氧化还原反应,置换出氢气 |
10.在N2+3H2?2NH3反应中,自反应开始至2s末,氨的浓度由0变为0.4mol/L,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
| A. | 0.3mol/(L•s) | B. | 0.4 mol/(L•s) | C. | 0.6 mol/(L•s) | D. | 0.8 mol/(L•s) |
17.下列属于链烃的是( )
| A. | CH3CH2Cl | B. | 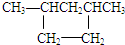 | C. | 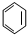 | D. | CH4 |
15.一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ,经测定完全吸收生成的二氧化碳需消耗5mol/L的KOH溶液200mL,恰好生成正盐.则此条件下反应:C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(g)的△H为( )
| A. | -16Q kJ/mol | B. | +8Q kJ/mol | C. | +16 Q kJ/mol | D. | -8 Q kJ/mol |
 ,
, .两种离子中,半径较小的是Na+(填离子符号).
.两种离子中,半径较小的是Na+(填离子符号). B2C2
B2C2 .
.
 +H2O;n HOCH2CH2OH+n HOOC-COOH
+H2O;n HOCH2CH2OH+n HOOC-COOH 
 +(2n-1)H2O.
+(2n-1)H2O. ③
③
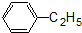 ⑤
⑤ ⑥
⑥