题目内容
20.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| C. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
分析 A、依据PH计算氢离子浓度,结合溶液中离子积常数计算碱溶液中氢氧根离子浓度,水溶液中水电离也生成氢氧根离子分析判断;
B、氯气与氢氧化钠溶液飞反应中,氯气既是氧化剂也是还原剂,属于歧化反应;
C、根据乙烯和丁烯的最简式都是CH2的特点来分析;
D、标况下,甲醇为液态.
解答 解:A、25℃时,pH=13的1.0L Ba(OH)2溶液中,碱含有的OH-数目为0.2NA,水存在电离生成氢氧根离子,所以溶液中氢氧根离子大于0.2NA,故A错误;
B、标况下2.24L氯气的物质的量为0.1mol,氯气与氢氧化钠的反应是歧化反应,因此0.1mol氯气与氢氧化钠溶液反应转移了0.1mol电子,转移的电子总数为0.1NA,故B错误;
C、乙烯和丁烯的最简式都是CH2,则$\frac{21g}{14g/mol}$,所以n(C)=1.5mol,N(C)=1.5NA,故C正确;
D、标况下,甲醇为液态,故不能根据气体摩尔体积来计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.常用的下列量器刻度表示正确的是( )
①量筒的刻度由下向上增大,无零刻度
②在250mL容量瓶上,除刻度线外,还标有250mL和20℃
③滴定管的刻度是由上向下增大,零刻度在上
④温度计的刻度由下向上增大,零刻度偏下
⑤用托盘天平称量样品质量时,指针应在标尺的中央.
①量筒的刻度由下向上增大,无零刻度
②在250mL容量瓶上,除刻度线外,还标有250mL和20℃
③滴定管的刻度是由上向下增大,零刻度在上
④温度计的刻度由下向上增大,零刻度偏下
⑤用托盘天平称量样品质量时,指针应在标尺的中央.
| A. | ②③正确 | B. | ①②⑤正确 | C. | 都正确 | D. | ②③④⑤正确 |
11.X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
(1)W位于元素周期表第三周期第ⅣA族;W的原子半径比X的大(填“大”或“小”).
(2)Z的第一电离能比W的小(填“大”或“小”); XY2由固态变为气态所需克服的微粒间作用力是分子间作用力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称CH3CH2OH、CH3COOH等.
(3)W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是Si+4HF=SiF4↑+2H2↑.
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(2)Z的第一电离能比W的小(填“大”或“小”); XY2由固态变为气态所需克服的微粒间作用力是分子间作用力;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称CH3CH2OH、CH3COOH等.
(3)W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是Si+4HF=SiF4↑+2H2↑.
8.已知2SO2(g)+O2(g)?2SO3(g).若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是( )
| A. | 升高温度,可以加快反应速率 | |
| B. | 使用催化剂是为了加快反应速率 | |
| C. | 在上述条件下,SO2不能完全转化为SO3 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度一定相等 |
5.关于反应中的先后顺序,下列评价正确的是( )
| A. | 向浓度都为0.1mol•L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应 | |
| B. | 向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 | |
| C. | 向浓度都为0.1mol•L-1的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应 | |
| D. | 向0.1mol•L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应 |
12.下列有关元素化合物的说法正确的是( )
| A. | 常温下,1mol铜片投入含有4mol HNO3的浓硝酸中,铜片可以完全溶解 | |
| B. | Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3 | |
| C. | 电解AlCl3、FeCl3、CuCl2的混合溶液中,阴极上依次析出Cu、Fe、Al | |
| D. | 反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,FeS2中的硫元素全部被氧化 |
4.下列图示试验正确的是( )
| A. |  制取收集干燥氨气 | B. |  碳酸氢钠受热分解 | ||
| C. |  除去CO气体中的CO2气体 | D. | 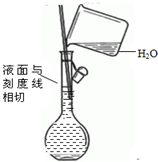 配制溶液 |
 .
. .
.
 .
.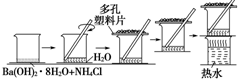 研究化学反应中的能量变化时,在一只小烧杯里,加入20g已研磨成粉末的Ba(OH)2•8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据下图所示实验步骤进行操作.回答下列问题:
研究化学反应中的能量变化时,在一只小烧杯里,加入20g已研磨成粉末的Ba(OH)2•8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据下图所示实验步骤进行操作.回答下列问题: