题目内容
【题目】已知X、Y是阳离子,Z是阴离子,M、N是分子,它们都由短周期元素组成,且具有以下结构特征和性质:
①X、Y、M、N的核外电子总数相等;②常温下,M是极易溶于N的气体;③X与M均由相同的元素组成;④Y为单核离子,其与Z组成的物质可用于净水;⑤Z由同主族元素组成。请回答下列问题:
(1)X的电子式为_______,Z的离子符号为_______。
(2)X与Z形成的化合物中所含有的化学键类型为_______。
(3)写出Y与M、N形成的混合物发生反应的离子方程式:_______。
【答案】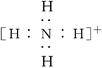 SO42- 离子键和共价键 Al3++3NH3·H2O=Al(OH)3↓+3NH4+
SO42- 离子键和共价键 Al3++3NH3·H2O=Al(OH)3↓+3NH4+
【解析】
根据题意可判断出X、Y、Z、M、N依次是NH4+、Al3+、SO42-、NH3、H2O。
(1)NH4+的电子式是 ,Z的离子符号是SO42-。
,Z的离子符号是SO42-。
(2)X与Z形成的化合物是(NH4)2SO4,其中含有离子键和共价键。
(3)M、N形成的混合物是氨水,Al3+与氨水反应的离子方程式为Al3++3NH3·H2O=Al(OH)3↓+3NH4+。

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目