题目内容
【题目】化合物J是一种香料,可按如下路线合成:

已知:
i.A的核磁共振氢谱有2组峰,峰面积之比为9:1;E为芳香烃。
ii.R-CH=CH2 ![]() R-CH2CH2OH
R-CH2CH2OH
iii.同一个碳上连两个羟基通常不稳定,易脱水形成碳氧双键
iv.R1CHO+R2CH2CHO![]()

试回答下列问题:
(1)A的化学名称为____________,I中所含的含氧官能团为__________(填名称)。
(2)反应②的反应类型为____________。
(3)H的分子式为_________________。
(4)H与新制Cu(OH)2悬浊液反应的化学方程式为_______________。
(5)满足下列条件的I的同分异构体共有_____种(不含立体异构)。
①含有苯环和碳碳双键
②能够发生银镜反应和水解反应
写出同分异构体中核磁共振氢谱图有5组峰,且峰面积之比为1:1:2:2:2的结构简式:________。
(6)参照上述合成路线以乙醇和甲醛为原料(无机试剂任选),设计制备丙烯酸(CH2=CHCOOH)的合成路线。______
【答案】异丁烷或2—甲基丙烷 羧基 消去反应 C9H8O  +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH +Cu2O↓+3H2O 5
+Cu2O↓+3H2O 5 ![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH2=CHCHO
CH2=CHCHO CH2=CHCOOH
CH2=CHCOOH
【解析】
A是一种气态烷烃,核磁共振氢谱只出现两组峰且峰面积之比为9:1,说明A的结构简式为(CH3)3CH,A与Cl2光照发生取代反应生成B(C4H9Cl),B在氢氧化钠醇溶液加热条件下发生消去反应生成C为(CH3)2C=CH2,C发生已知ii的反应生成D为(CH3)2CHCH2OH;E为芳香烃,说明E为甲苯,甲苯与Cl2光照发生取代反应生成F为C6H5CHCl2,结合已知iii,F发生水解反应生成G为C6H5CHO,G发生已知iv的反应生成H为C6H5CH=CHCHO,H发生氧化反应生成I为C6H5CH=CHCOOH;D和I发生酯化反应生成J为C6H5CH=CHCOOCH2CH(CH3)2,据此解答。
(1)根据上面的分析可知,A为(CH3)3CH,化学名称为异丁烷或2—甲基丙烷,I为C6H5CH=CHCOOH,I中所含的含氧官能团为羧基。
故答案为:异丁烷或2—甲基丙烷;羧基;
(2)反应②为卤代烃的消去反应,
故答案为:消去反应;
(3)H为C6H5CH=CHCHO,分子式为C9H8O,
故答案为:C9H8O;
(4)H为C6H5CH=CHCHO,H与新制Cu(OH)2悬浊液反应的化学方程式为![]() ,
,
故答案为:![]() ;
;
(5)I为C6H5CH=CHCOOH,其同分异构体,同时具有以下特征:①含有苯环和碳碳双键 ②能够发生银镜反应和水解反应,说明含有甲酸形成的酯基,苯环上有一个取代基为HCOOCH=CH-或![]() 有2种,含有2个取代基为HCOO-、CH2=CH-,有邻、间、对3种位置,共有5种结构,其中核磁共振氢谱图有5组峰,且峰面积之比为1:1:2:2:2的结构简式为:
有2种,含有2个取代基为HCOO-、CH2=CH-,有邻、间、对3种位置,共有5种结构,其中核磁共振氢谱图有5组峰,且峰面积之比为1:1:2:2:2的结构简式为:![]() ,
,
故答案为:5;![]() ;
;
(6)参照上述合成路线,若要制备丙烯酸(CH2=CHCOOH),可先制得CH2=CHCHO,根据题中已知iv的反应,可用CH3CHO与HCHO反应制备CH2=CHCHO,而CH3CHO可用原料乙醇催化氧化制备,故合成路线设计为:CH3CH2OH ![]() CH3CHO
CH3CHO![]() CH2=CHCHO
CH2=CHCHO CH2=CHCOOH,
CH2=CHCOOH,
故答案为:CH3CH2OH ![]() CH3CHO
CH3CHO![]() CH2=CHCHO
CH2=CHCHO CH2=CHCOOH。
CH2=CHCOOH。

 初中暑期衔接系列答案
初中暑期衔接系列答案【题目】碳酸亚铁(白色固体,难溶于水)是一种重要的工业原料,可用于制备补血剂乳酸亚铁,也可用作可充电电池的电极。某研究小组通过下列实验,寻找利用复分解反应制备FeCO3的最佳方案:
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
| 0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L Na2CO3溶液 (pH=11.9) | 实验Ⅰ:立即产生灰绿色沉淀,5min后出现明显的红褐色 |
0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L NaHCO3溶液 (pH=8.6) | 实验Ⅱ:产生白色沉淀及少量无色气泡,2min后出现明显的灰绿色 | |
0.8 mol/L (NH4)2Fe(SO4)2 溶液(pH=4.0) | 1 mol/L NaHCO3溶液 (pH=8.6) | 实验Ⅲ:产生白色沉淀及无色气泡,较长时间保持白色 | |
(1)实验I中红褐色沉淀产生的原因可用如下反应表示,请补全反应:_____________
![]() Fe2++
Fe2++ ![]() +
+ ![]() +
+ ![]() H2O
H2O ![]()
![]() Fe(OH)3 +
Fe(OH)3 + ![]() HCO3
HCO3
(2)实验II中产生FeCO3的离子方程式为__________________。
(3)为了探究实验III中NH4+所起的作用,甲同学设计了实验IV进行探究:
操作 | 现象 | |
实验IV | 向0.8 mol/L FeSO4溶液中加入________,再加入一定量Na2SO4固体配制成混合溶液(已知Na+对实验无影响,忽略混合后溶液体积变化)。再取该溶液一滴管,与2mL 1mol/L NaHCO3溶液混合 | 与实验III现象相同 |
实验IV中加入Na2SO4固体的目的是_________。
对比实验II、III、IV,甲同学得出结论:NH4+水解产生H+,降低溶液pH,减少了副产物Fe(OH)2的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是:_________,再取该溶液一滴管,与2mL 1mol/L NaHCO3溶液混合。
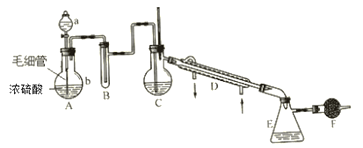
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验III中FeCO3的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验I、II、III中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。

① 补全A中装置并标明所用试剂。____________
② 为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是____________。
(5)实验反思:经测定,实验III中的FeCO3纯度高于实验I和实验II。通过以上实验分析,制备FeCO3实验成功的关键因素是____________。