题目内容
【题目】对于可逆反应:mA(g)+nB(g)![]() pC(g)+qD(g) ΔH=?,反应物A的转化率随时间和温度的变化如下图所示,下列判断正确的是
pC(g)+qD(g) ΔH=?,反应物A的转化率随时间和温度的变化如下图所示,下列判断正确的是
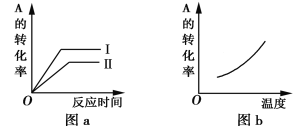
A. 由图b可知,ΔH<0
B. 图a中要使平衡状态Ⅱ到平衡状态Ⅰ,可以加入催化剂
C. 若m+n>p+q,则由状态Ⅱ到状态Ⅰ可以压缩容器体积
D. 在不同的平衡状态Ⅰ和Ⅱ时,化学平衡常数一定相同
【答案】C
【解析】
根据外因对化学反应速率和化学平衡的影响分析判断。
A项:由图b可知,温度升高,A的转化率变大,即升温平衡右移,故正反应ΔH>0,A项错误;
B项:图a中平衡状态Ⅱ、平衡状态Ⅰ的A转化率不同,即平衡状态不同,而催化剂不能使平衡移动,B项错误;
C项:图a中曲线I先达到化学平衡,可能是压强较大。当m+n>p+q时,增加压强(压缩容器体积)平衡右移,则由状态Ⅱ可以到达状态Ⅰ,C项正确;
D项:图a中曲线I先达到化学平衡,也可能是温度较高。在不同的平衡状态Ⅰ和Ⅱ时,化学平衡常数可能不同,D项错误。
本题选C。

 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案【题目】向1L含0.01molNaAlO2和0.02molNaOH的溶液中缓慢通入二氧化碳,随n(CO2)增大,先后发生三个不同的反应,当0.01mol<n(CO2) ![]() 0.015时发生的反应是:2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3下列对应关系正确的是( )
0.015时发生的反应是:2 NaAlO2+ CO2+2H2O=2Al(OH)3↓+Na2CO3下列对应关系正确的是( )
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)> c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)> c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)> c(HCO3-)> c(OH-)>c(H+) |
A. A B. B C. C D. D