题目内容
19.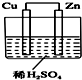 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )实验后的记录:
①Cu为负极,Zn为正极 ②Cu极上发生还原反应
③SO${\;}_{4}^{2-}$向Zn极移动 ④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu-→Zn ⑥正极反应式:Cu+2e-═Cu2+,发生氧化反应.
| A. | ①②⑥ | B. | ②③④ | C. | ②③⑥ | D. | ③④⑤ |
分析 Zn-Cu原电池中,Zn作负极,发生电池反应Zn+2H+=Zn2++H2↑,电子由负极流向正极,阴离子向负极移动,以此来解答.
解答 解:①Zn为负极,Cu为正极,故①错误;
②Cu电极上发生2H++2e-=H2↑,所以Cu极上有气泡产生,发生还原反应,故②正确;
③SO42-向负极锌极移动,故③正确;
④由2H++2e-=H2↑可知,有0.5mol电子流向导线,产生氢气0.25mol,故④正确;
⑤电子由Zn电极流向Cu电极,故⑤错误;
⑥正极反应为2H++2e-=H2↑,故⑥错误;
故选B.
点评 本题考查原电池,为高频考点,明确电极的判断、发生的电极反应、电子、离子的移动方向即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( )
| A. | 丙烷与氯气在光照的作用下的反应 | B. | 乙烯与溴的四氯化溶液的反应 | ||
| C. | 乙烯与水的反应 | D. | 乙烯自身生成聚乙烯的反应 |
7.下列说法不正确的是( )
| A. | 淀粉、纤维素、蛋白质在一定条件下均能发生水解反应,水解产物不相同 | |
| B. | 汽油、油脂不一定能使酸性高锰酸钾溶液褪色 | |
| C. | 煤的干馏、石油催化重整、石油裂化、煤的液化都属于化学变化 | |
| D. | 甘氨酸和谷氨酸在一定条件下最多能形成三种二肽 |
14.下列有关金属腐蚀与防护的说法不正确的是( )
| A. | 钢铁在弱碱性条件下发生电化学腐蚀的正极反应是:O2+2H2O+4e-═4OH- | |
| B. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| D. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
4.有关l3C、15N的下列说法正确的是( )
| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同素异形体 | ||
| C. | 15N与14N互为同位素 | D. | 15N和14N的化学性质不同 |
11.下列物质既能与KMnO4酸性溶液反应,又能与溴水反应的一组物质是( )
①苯 ②苯酚 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸.
①苯 ②苯酚 ③甲苯 ④乙醇 ⑤己烯 ⑥己烷 ⑦亚硫酸.
| A. | ②③⑤⑥ | B. | ②④⑥⑦ | C. | ②⑤⑦ | D. | 全部 |
8.下列排列顺序正确的是( )
| A. | 微粒半径:Na+>K+>Cl->S2- | B. | 稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO4 | D. | 熔点:Al>Mg>Na>K |
9.下列含有非极性键的共价化合物是( )
| A. | HCl | B. | Na2O2 | C. | N2H4 | D. | CH4 |