题目内容
4.有关l3C、15N的下列说法正确的是( )| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同素异形体 | ||
| C. | 15N与14N互为同位素 | D. | 15N和14N的化学性质不同 |
分析 A.元素左上角数字表示质量数,中子数=质量数-质子数;
B.同一元素的不同单质互称同素异形体;
C.质子数相同中子数不同的同一元素互称同位素;
D.元素的化学性质主要和原子的最外层电子数有关;
解答 解:A.13C与15N有相同的中子数分别为:13-6=7,15-7=8,两者不相等,故A错误;
B.13C为原子,C60为单质,二者不是同素异形体,故B错误;
C.14N与15N的质子数都为7,中子数分别为14-7=7,15-7=8,两者不同,属于同位素,故C正确;
D.元素的化学性质主要和原子的最外层电子数有关,15N和14N的核外电子排布相同,化学性质相似,故D错误;
故选C.
点评 本题考查原子中的数量关系,明确质子数、中子数、质量数的关系,质子数与电子数的关系以及同位素、同素异形体的概念及判断是解答关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
14.下列关于甲烷的叙述中错误的是( )
| A. | 甲烷分子具有正四面体结构,两个碳氢键之间的夹角为109°28′ | |
| B. | 甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 | |
| C. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 | |
| D. | “抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
15.在Na2CO3和HCl反应的下列各组实验中,反应速率最快的一组是( )
| 组号 | 温度(℃) | Na2CO3浓度(mol/L) | HCl浓度(mol/L) |
| A | 0 | 0.1 | 0.1 |
| B | 20 | 0.1 | 0.1 |
| C | 40 | 0.1 | 0.2 |
| D | 40 | 0.2 | 0.2 |
| A. | A | B. | B | C. | C | D. | D |
12.最近医学界通过用放射性15C跟踪标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),则有关15C的叙述正确的是( )
| A. | 与C60中普通碳原子的化学性质不同 | |
| B. | 与16O的中子数相同 | |
| C. | 与12C互为同位素 | |
| D. | 是足球烯的同素异形体 |
9.元素周期表可以划分为5个区,下列有关说法正确的是( )
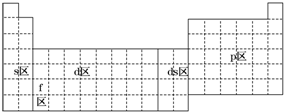

| A. | s区全部是金属元素 | |
| B. | p区全部是非金属元素 | |
| C. | d区内元素原子的价电子排布必为(n-1)d1~10ns2 | |
| D. | 除ds区外,以最后填入电子的轨道能级符号作为区的符号 |
13.下列离子方程式,正确的是( )
| A. | 过氧化钠与水反应:2O22-+2H2O═4OH-+O2↑ | |
| B. | 澄清石灰水中通入过量二氧化碳:OH-+CO2═HCO3- | |
| C. | 往FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+ | |
| D. | CaCO3溶于稀盐酸中:CO32-+2H+═CO2↑+H2O |
14.下列反应的离子方程式正确的是( )
| A. | 铁跟氯化铁溶液反应:Fe+2Fe3+=3Fe2+ | |
| B. | 氨水跟盐酸反应:OH-+H+→H2O | |
| C. | 氢氧化钡跟稀硫酸反应:Ba2++OH-+H++SO42-→BaSO4↓+H2O | |
| D. | 碳酸钙跟盐酸反应:CO32-+2H+→CO2↑+H2O |
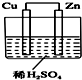 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( ) 和
和