题目内容
9.写出有关化学方程式:(1)金属铜与稀硝酸反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(2)两只棉球分别滴有几滴浓氨水和浓盐酸放入同一只烧杯中,用表面皿盖住烧杯口,烧杯内有白烟:NH3+HCl=NH4Cl;
(3)一瓶无色气体打开瓶盖后,瓶口呈现出红棕色:2NO+O2=2NO2.
分析 (1)硝酸是氧化性酸,金属铜与稀硝酸反应,氧化剂是硝酸、还原剂是Cu,反应生成硝酸铜、NO和水;
(2)氨水、浓盐酸易挥发,二者反应生成白烟氯化铵固体;
(3)一氧化氮易被氧气氧化,无色的NO气体挥发到空气中与O2反应,瓶口呈现出红棕色,说明生成二氧化氮气体.
解答 解:(1)稀硝酸和铜反应生成硝酸铜、NO和水,反应方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(2)氨水、浓盐酸易挥发,二者反应NH3+HCl=NH4Cl,生成氯化铵固体,形成白烟,故答案为:NH3+HCl=NH4Cl;
(3)瓶口呈现出红棕色,说明生成二氧化氮气体,瓶内含有无色的NO,反应为2NO+O2=2NO2,故答案为:2NO+O2=2NO2.
点评 本题综合考查元素化合物知识,为高考高频考点,侧重于有关氮元素的基础知识的综合理解和运用的考查,注意相关基础知识的积累,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列各组混合物中,可以用分液漏斗分离的是( )
| A. | 溴乙烷和水 | B. | 苯酚和乙醇 | C. | 酒精和水 | D. | 乙醛和苯 |
17.下列性质适合于离子晶体的是( )
| A. | 熔点-218℃,难溶于水 | |
| B. | 熔点3 900℃,硬度很大,不导电 | |
| C. | 难溶于水,固体时导电,升温时导电能力减弱 | |
| D. | 难溶于水,熔点高,固体不导电,熔化时导电 |
4.一定质量的某有机物与足量金属钠反应要得VAL气体.相同质量的该有机物与足量的NaHCO3浓溶液反应,可得VBL气体.已知在同温同压下VA和VB相同,则该有机物可能是( )
| A. | CH3CH(OH)COOH | B. | HOOC-COOH | ||
| C. | CH3CH2CH2OH | D. |  |
14.下列关于甲烷的叙述中错误的是( )
| A. | 甲烷分子具有正四面体结构,两个碳氢键之间的夹角为109°28′ | |
| B. | 甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 | |
| C. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 | |
| D. | “抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
1.下列有关物质用途的说法中,不正确的是( )
| A. | 四氯化碳可做有机溶剂 | |
| B. | 可用工业酒精勾兑白酒 | |
| C. | 甲烷是清洁高效的燃料 | |
| D. | 用二氯甲烷只有一种结构证明甲烷空间结构是正四面体 |
18.下列粒子的结构示意图中,表示钠离子( )
| A. | 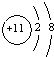 | B. | 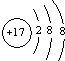 | C. | 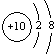 | D. | 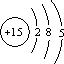 |
 ,若该烷烃可由3种单烯烃与H2加成得到,则该烯烃可能的结构简式是CH2=C(CH3)CH2CH3、(CH3)2C=CHCH3、(CH3)2CHCH=CH2.
,若该烷烃可由3种单烯烃与H2加成得到,则该烯烃可能的结构简式是CH2=C(CH3)CH2CH3、(CH3)2C=CHCH3、(CH3)2CHCH=CH2.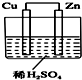 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )