题目内容
【题目】X、Y、Z、W四种元素的部分信息如下表所示。
元素 | X | Y | Z | W |
相关 信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应 |
回答下列问题:
(1)W的基态原子电子排布式为___,X、Y、Z三种元素电负性由大到小的顺序为___(用具体的元素符号填写)。
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型不是sp3杂化的是___ (填化学式,下同),分子构型是正四面体的是___,ZX3属于___(极性分子、非极性分子)。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为___。
(4)Z原子的价电子轨道表示式为___。
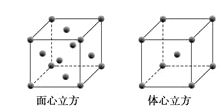
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为___;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为___gcm-3。
【答案】[Ar]3d64s2 Cl>P>C PCl5 CCl4 极性分子 分子晶体 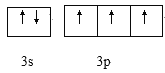 12
12 ![]()
【解析】
根据题干信息:X是短周期元素,最高化合价为+7价,故X为Cl,Y的基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子即1s22s22p2,故Y是C,Z的核外电子共有15种运动状态,即含有15个电子,故Z是P,W能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应,故W是Fe。
(1)Fe是26号元素,故基态原子电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2,根据同一周期从左往右电负性增大,可知Cl、C、P三种元素电负性由大到小的顺序为Cl>P>C ,故答案为:1s22s22p63s23p63d64s2或[Ar]3d64s2 Cl>P>C;
(2)化合物CCl4是sp3杂化是正四面体构型,PCl3是sp3杂化是三角锥型、PCl5(气态或液态时)P原子周围形成了五个σ键故不是sp3杂化是三角双锥构型,故中心原子的轨道类型不是sp3杂化的是PCl5,分子构型是正四面体的是CCl4,PCl3空间构型是三角锥型,故其属于极性分子,故答案为:PCl5 CCl4 极性分子 ;
(3)根据FeCl3的熔点、沸点较低,可知则FeCl3的晶体类型为分子晶体,故答案为:分子晶体;
(4)P原子的价电子轨道表示式为![]() 。
。
(5)金属晶体中原子的配位数是指离某原子距离相等且最近的原子个数,Fe元素的面心立方晶胞的单质中Fe原子的配位数为相互垂直的三个面上的四个原子,即配位数是12;体心立方晶体中,假设晶胞的边长为a,则有:![]() ,即
,即![]() ,又1个晶胞中含有
,又1个晶胞中含有![]() ,故晶胞的密度为:
,故晶胞的密度为:![]()
 ,故答案为:
,故答案为:![]() 。
。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案【题目】(1)某学生用标准盐酸滴定待测的NaOH溶液,根据3次实验分别记录有关数据如表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
则依据表中数据,该NaOH溶液的物质的量浓度为______。
(2)实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作可能使测定结果偏低的是______。
A.酸式滴定管用蒸馏水洗涤后未用标准液清洗
B.开始实验时,酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.滴定过程中,锥形瓶内溶液颜色由黄色变为橙色,但又立即变为黄色,此时便停止滴定,记录读数
D.达到滴定终点时,仰视读数并记录
(3)准确量取25.00mL酸性高锰酸钾溶液应用______。(填仪器名称)