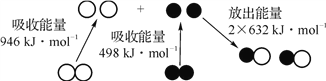
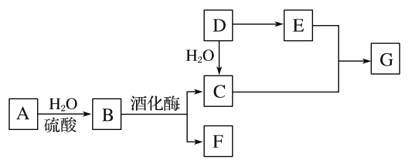
题目内容
【题目】(1)某学生用标准盐酸滴定待测的NaOH溶液,根据3次实验分别记录有关数据如表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
则依据表中数据,该NaOH溶液的物质的量浓度为______。
(2)实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作可能使测定结果偏低的是______。
A.酸式滴定管用蒸馏水洗涤后未用标准液清洗
B.开始实验时,酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.滴定过程中,锥形瓶内溶液颜色由黄色变为橙色,但又立即变为黄色,此时便停止滴定,记录读数
D.达到滴定终点时,仰视读数并记录
(3)准确量取25.00mL酸性高锰酸钾溶液应用______。(填仪器名称)
【答案】0.1044mol/L C 酸式滴定管
【解析】
(1)先根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸);
(2)利用c(碱)=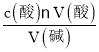 来进行浓度计算;
来进行浓度计算;
(3)高锰酸钾具有氧化性,所以准确量取25.00mL酸性高锰酸钾溶液应用酸式滴定管。
(1)由三次盐酸溶液的体积可知,第2组数据偏差太大,要舍去,求出1、3组平均消耗盐酸平均体积值V(盐酸)=![]() mL=26.10mL,由HCl与NaOH反应方程式HCl+NaOH=NaCl+H2O,可知c(碱)=
mL=26.10mL,由HCl与NaOH反应方程式HCl+NaOH=NaCl+H2O,可知c(碱)=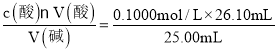 =0.1044mol/L;
=0.1044mol/L;
(2)由c(碱)=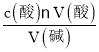 可知:
可知:
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,消耗酸的体积增大,则c(碱)偏大,A不符合题意;
B.酸式滴定管在滴定前有气泡,滴定后气泡消失,消耗酸的体积增大,则c(碱)偏大,B不符合题意;
C.滴定过程中,锥形瓶内溶液颜色由黄色变为橙色,但又立即变为黄色,此时便停止滴定,记录读数,实际上加入的标准液体积偏小,导致待测碱液浓度偏低,C符合题意;
D.读取盐酸体积时,仰视读数记录,读数偏大,则消耗酸的体积偏大,导致待测液溶液c(碱)偏高,D不符合题意;
故合理选项是C;
(3)酸性高锰酸钾溶液具有强的氧化性,容易腐蚀碱式滴定管的橡胶管,所以准确量取25.00mL酸性高锰酸钾溶液应用酸式滴定管。

【题目】X、Y、Z、W四种元素的部分信息如下表所示。
元素 | X | Y | Z | W |
相关 信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应 |
回答下列问题:
(1)W的基态原子电子排布式为___,X、Y、Z三种元素电负性由大到小的顺序为___(用具体的元素符号填写)。
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型不是sp3杂化的是___ (填化学式,下同),分子构型是正四面体的是___,ZX3属于___(极性分子、非极性分子)。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为___。
(4)Z原子的价电子轨道表示式为___。
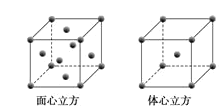
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为___;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为___gcm-3。