题目内容
15.下列制备实验不可能成功的是( )| A. | 将冰醋酸、乙醇和浓硫酸混合共热制取乙酸乙酯 | |
| B. | 将乙醇和3mol/L的硫酸按体积比1:3混合共热至170℃制乙烯 | |
| C. | 蔗糖在酸性条件下水解后与新制的氢氧化铜共热能看到红色沉淀 | |
| D. | 用苯、液溴和还原铁粉制溴苯 |
分析 A.冰醋酸、乙醇和浓硫酸发生酯化反应;
B.3mol/L的硫酸不是浓硫酸;
C.蔗糖在酸性条件下水解后生成葡萄糖,葡萄糖具有还原性;
D.苯、液溴和还原铁粉,发生取代反应生成溴苯和HBr.
解答 解:A.冰醋酸、乙醇和浓硫酸发生酯化反应生成乙酸乙酯,浓硫酸作催化剂和吸水剂,故A正确;
B.3mol/L的硫酸不是浓硫酸,应利用乙醇与浓硫酸混合共热至170℃制乙烯,故B错误;
C.蔗糖在酸性条件下水解后生成葡萄糖,葡萄糖具有还原性,可与新制的氢氧化铜共热生成氧化亚铜沉淀,则能看到红色沉淀,故C正确;
D.苯、液溴和还原铁粉,发生取代反应生成溴苯和HBr,Fe(或溴化铁)在反应中作催化剂,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的制备实验及有机物的性质等,把握性质及发生的反应为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C═K2S+N2↑+3CO2↑.该反应中氧化剂是( )
| A. | S | B. | KNO3 | C. | C | D. | CO2 |
6.设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A. | 常温常压下,1mol固体氢氧化钠的体积比1mol氢气的体积小 | |
| B. | NA个氧气分子和NA个氢气分子的质量比为16:l | |
| C. | 28g氮气所含的原子数目为NA | |
| D. | NA个H2SO4分子中所含氧原子个数与4NA个H2O分子中所含氧原子个数相等 |
3.把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是( )
| A. | 稀H2SO4 | B. | CuSO4溶液 | C. | AgNO3溶液 | D. | Fe2(SO4)3溶液 |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,16g O2和32g O3的混合物中,含有O原子数目为3NA | |
| B. | 标准状态下,1mol Na2O和1mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1mol NaHSO4溶于水或受热熔化,电离出来的离子数目均为2NA | |
| D. | 在K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O中,若生成71g Cl2,转移的电子数目为$\frac{5}{3}$NA |
7.下列物质中,既能发生消去反应,又能催化氧化生成醛的是( )
| A. | CH3OH | B. | C2H5OH | C. | (CH3)3COH | D. | (CH3)3CCH2OH |
9.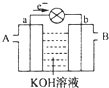 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )| A. | a电极发生还原反应,b电极发生氧化反应 | |
| B. | a电极的电极反应式为:CO+4OH-+2e-=CO2+2H2O | |
| C. | A处通入的是空气,B处通入的是CO | |
| D. | 用这种电池作电源精炼铜,若阴极质量增加6.4 g,则至少消耗标准状况下的CO 2.24 L |
10.下列物质中,与CH3-CH=CH-CH3互为同分异构体的是( )
| A. | CH3CH2CH2CH3 | B. | 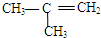 | C. | 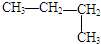 | D. | CH3-CH=CH2 |