题目内容
5.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C═K2S+N2↑+3CO2↑.该反应中氧化剂是( )| A. | S | B. | KNO3 | C. | C | D. | CO2 |
分析 该反应中,硫元素化合价由0价变为-2价,N元素化合价由+5价变为0价,碳元素化合价由0价变为+4价,根据元素化合价变化判断氧化剂和还原剂,氧化剂在反应中被还原,还原剂在反应中被氧化,以此解答.
解答 解:反应S+2KNO3+3C═K2S+N2↑+3CO2↑中,S元素化合价由0价降低到-2价,则S为氧化剂,N元素化合价由+5价降低到0价,则KNO3为氧化剂,C元素化合价由0价升高到+4价,则C为还原剂,
故选AB.
点评 本题考查氧化还原反应,把握变化中元素的化合价为解答的关键,侧重氧化还原反应基本概念及电子转移的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
相关题目
16.下列物质的分类组合正确的是( )
| A | B | C | D | |
| 化合物 | HCl | NaOH | Cu2(OH)2SO4 | FeSO4•7H2O |
| 氧化物 | H2O | Na2O | CO | Fe3O4 |
| 电解质 | 浓盐酸 | 纯碱 | 胆矾溶液 | 铁 |
| A. | A | B. | B | C. | C | D. | D |
13.在Fe(NO3)2溶液中存在下列平衡:Fe2++2H2O?2Fe(OH)2+2H+,又已知Fe2+的颜色为浅绿色.现向该溶液中加入稀盐酸,则溶液的颜色为( )
| A. | 无变化 | B. | 变为无色 | C. | 变为深绿色 | D. | 变为棕黄色 |
20.下列实验现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Cu片放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | Al2(SO4)3溶液中滴加过量氨水 | 生成白色胶状物质 | Al(OH)3不溶于氨水 |
| C | 向某溶液中加入新制氯水,再向溶液中加入KSCN溶液 | 溶液变红色 | 该溶液中含有Fe2+ |
| D | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I- |
| A. | A | B. | B | C. | C | D. | D |
17.在一定温度下,在恒容的密闭容器中进行的可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A. | C生成的速率和C分解的速率相等 | |
| B. | 单位时间内生成n mol A,同时生成3n mol B | |
| C. | B的消耗速率与C的消耗速率之比为1:1 | |
| D. | 混合气体密度保持不变 |
14.下列化学用语使用正确的是( )
| A. | NH4Cl的电子式: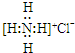 | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | 氟化钠的电子式: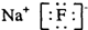 | |
| D. | 氯原子的结构示意图: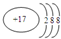 |
15.下列制备实验不可能成功的是( )
| A. | 将冰醋酸、乙醇和浓硫酸混合共热制取乙酸乙酯 | |
| B. | 将乙醇和3mol/L的硫酸按体积比1:3混合共热至170℃制乙烯 | |
| C. | 蔗糖在酸性条件下水解后与新制的氢氧化铜共热能看到红色沉淀 | |
| D. | 用苯、液溴和还原铁粉制溴苯 |
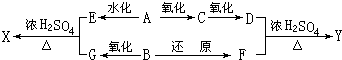
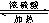 HCOOC2H5+H2O.
HCOOC2H5+H2O.