题目内容
17.在三个密闭容器中分别充入N2、H2、HCl三种气体,当它们的温度和密度都相同时,这三种气体的压强(p),从大到小的顺序是( )| A. | p(N2)>p(H2)>p(HCl) | B. | p(HCl)>p(N2)>p(H2) | C. | p(H2)>p(HCl)>p(N2) | D. | p(H2)>p(N2)>p(HCl) |
分析 由PV=nRT=$\frac{m}{M}$RT,则PM=ρRT,相同温度、密度下,压强与摩尔质量成反比.
解答 解:由PV=nRT=$\frac{m}{M}$RT,则PM=ρRT,相同温度、密度下,压强与摩尔质量成反比,由于摩尔质量M(HCl)>M(N2)>M(H2),故压强:p(H2)>p(N2)>p(HCl),故选:D.
点评 本题考查阿伏伽德罗定律及其推论,注意根据由PV=nRT理解阿伏伽德罗定律及其推论,难度不大.

练习册系列答案
相关题目
5. 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g)+H2O (g)?CO2(g)+H2 (g)△H<0
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g)+H2O (g)?CO2(g)+H2 (g)△H<0
(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率
v(CO2)=0.03mol•L-1•min-1
(2)t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如表:
①计算t1℃该反应的平衡常数为 k=0.5,t1℃大于850℃(填“大于”、“小于”或“等于”).判断依据是:正反应为放热反应.
②t1℃时,反应在4min~5min间,平衡向左移动(填“向左”、“向右”或“不移动”),可能的原因是b.
a.增加CO的浓度 b.增加H2的浓度 c.加压 d.使用催化剂.
 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g)+H2O (g)?CO2(g)+H2 (g)△H<0
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g)+H2O (g)?CO2(g)+H2 (g)△H<0(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率
v(CO2)=0.03mol•L-1•min-1
(2)t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如表:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②t1℃时,反应在4min~5min间,平衡向左移动(填“向左”、“向右”或“不移动”),可能的原因是b.
a.增加CO的浓度 b.增加H2的浓度 c.加压 d.使用催化剂.
2.下列物质混合后,不会发生离子反应的是( )
| A. | NaOH溶液和FeCl3溶液 | B. | Na2CO3溶液和稀硫酸 | ||
| C. | CuSO4溶液和Ba(OH)2溶液 | D. | Na2SO4溶液和MgCl2溶液 |
9.同温同压下,甲容器中的NH3和乙容器中的CH4所含的原子总数相同,则甲容器与乙容器的体积之比为( )
| A. | 1:1 | B. | 2:1 | C. | 3:4 | D. | 5:4 |
6.有关煤的综合利用如图所示.下列说法正确的是( )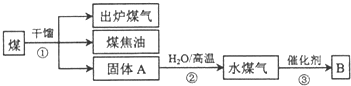

| A. | 煤和水煤气均是二次能源 | |
| B. | 煤中含有苯、甲苯、二甲苯等有机物 | |
| C. | ①是将煤在空气中加强热使其分解的过程 | |
| D. | B为甲醇或乙酸时,原子利用率均达到100% |