题目内容
19.为了减少二氧化碳等温室气体的排放,科学家采取“组织转化”技术,将CO2和H2在催化剂和加热条件喜爱转化为一种重要的化工原料乙烯(C2H4)和H2O,反应化学方程式为2CO2+6H2$\frac{\underline{\;催化剂\;}}{\;}$C2H4+4H2O.若要制得28gC2H4,需要CO2的质量是多少?分析 根据方程式2CO2+6H2$\frac{\underline{\;催化剂\;}}{\;}$C2H4+4H2O中质量定比关系计算二氧化碳质量.
解答 解:设需要CO2的质量为m,则:
2CO2+6H2$\frac{\underline{\;催化剂\;}}{\;}$C2H4+4H2O
88 28
m 28g
所以m=$\frac{88×28g}{28}$=88g
答:需要CO2的质量88g.
点评 本题考查化学方程式计算,比较基础,注意对化学方程式意义的理解掌握.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目
9.某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2mol该离子恰好能使0.6molSO32-离子完全氧化为SO42-,则X2O72-离子还原后的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
10.朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”月光穿过薄雾所形成的种种美景的本质原因是( )
| A. | 青雾中的小水滴颗粒大小约为10-9m~10-7m | |
| B. | 光是一种胶体 | |
| C. | 雾是一种胶体 | |
| D. | 发生丁达尔效应 |
7.对于可逆反应:mA(g)+nB(g)?xC(g)+yD(s)△H=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如图所示,下列判断正确的是( )


| A. | △H>0,m+n>x+y | B. | △H<0,m+n>x+y | C. | △H<0,m+n>x | D. | △H>0,m+n<x |
4.下列化学方程式中,电子转移不正确的是( )
| A. |  | |
| B. |  | |
| C. |  | |
| D. |  |
16.卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子.若以它以及表2中的某些物质为原料,按图所示工艺流程进行生产,可制得轻质氧化镁.
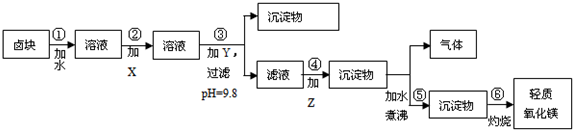
若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
*Fe2+氢氧化物呈絮状,不易从溶液中除去,所以,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去.
表2 原料价格表
(1)在步骤②中加入的试剂X,最佳的选择是漂液NaClO,写出步骤②中pH=1时所发生反应的离子方程式:2Fe2++ClO-+2H+═2Fe3++Cl-+H2O;
(2)在步骤③中加入的试剂是烧碱;之所以要控制pH=9.8,其目的是使Mg2+以外的杂质离子转化成沉淀除去;
(3)某燃料电池的燃料为CO,氧化剂为含CO2的O2,电解质为熔融态的试剂Z(步骤④中加入试剂的有效成分),则该燃料电池的正极电极反应方程式为:O2+4e-+2CO2═2CO32-;
(4)在步骤⑤中发生的反应是MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$ Mg(OH)2+CO2↑.

若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6* |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2 原料价格表
| 物质 | 价格(元•吨-1) |
| 漂液(含25.2% NaClO) | 450 |
| 双氧水(含30% H2O2) | 2400 |
| 烧碱(含98% NaOH) | 2100 |
| 纯碱(含99.5% Na2CO3) | 600 |
(2)在步骤③中加入的试剂是烧碱;之所以要控制pH=9.8,其目的是使Mg2+以外的杂质离子转化成沉淀除去;
(3)某燃料电池的燃料为CO,氧化剂为含CO2的O2,电解质为熔融态的试剂Z(步骤④中加入试剂的有效成分),则该燃料电池的正极电极反应方程式为:O2+4e-+2CO2═2CO32-;
(4)在步骤⑤中发生的反应是MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$ Mg(OH)2+CO2↑.
17.在三个密闭容器中分别充入N2、H2、HCl三种气体,当它们的温度和密度都相同时,这三种气体的压强(p),从大到小的顺序是( )
| A. | p(N2)>p(H2)>p(HCl) | B. | p(HCl)>p(N2)>p(H2) | C. | p(H2)>p(HCl)>p(N2) | D. | p(H2)>p(N2)>p(HCl) |
 向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题: