题目内容
1.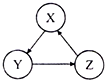 下列各组物质,不能按照图关系相互转化的是(“→”表示反应一步完成)( )
下列各组物质,不能按照图关系相互转化的是(“→”表示反应一步完成)( )| 选项 | X | Y | Z |
| A | Fe | FeCl3 | FeCl2 |
| B | HCl | Cl2 | HClO |
| C | S | SO3 | H2SO4 |
| D | HNO3 | NO | NO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、Fe$\stackrel{氯气}{→}$FeCl3$\stackrel{铁}{→}$FeCl2$\stackrel{锌}{→}$Fe;
B、HCl$\stackrel{二氧化锰}{→}$Cl2$\stackrel{水}{→}$HClO$\stackrel{光照}{→}$HCl;
C、硫不能一步生成三氧化硫;
D、HNO3$\stackrel{铜}{→}$NO$\stackrel{氧气}{→}$NO2$\stackrel{水}{→}$HNO3.
解答 解:A、Fe$\stackrel{氯气}{→}$FeCl3$\stackrel{铁}{→}$FeCl2$\stackrel{锌}{→}$Fe,可以按如图“→”一步完成,故A正确;
B、HCl$\stackrel{二氧化锰}{→}$Cl2$\stackrel{水}{→}$HClO$\stackrel{光照}{→}$HCl,可以按如图“→”一步完成,故B正确;
C、硫不能一步生成三氧化硫,硫与氧气反应只能生成二氧化硫,所以不能实现按如图“→”一步完成,故C错误;
D、HNO3$\stackrel{铜}{→}$NO$\stackrel{氧气}{→}$NO2$\stackrel{水}{→}$HNO3,可以按如图“→”一步完成,故D正确;
故选C.
点评 本题考查了物质之间通过一步反应的原理,根据常见化学物质的性质,通过列举具体反应,判断物质间是否可以实现一步反应的转化,采用排除法(即发现一步转化不能实现,排除该选项)是解答本题的捷径,题目难度中等.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
11.下列说法正确的是( )
| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | |
| C. | 第3周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
9.下列叙述正确的是( )
| A. | 加碘食盐,能使淀粉显蓝色 | |
| B. | 非金属氧化物一定为酸性氧化物 | |
| C. | 浓硝酸和浓硫酸与铜反应都能表现出强氧化性和酸性 | |
| D. | 实验室可用氯化铵固体与氢氧化钠固体共热制氨气 |
16.向某溶液中加入BaCl2溶液,出现白色沉淀,再加入稀硝酸,白色沉淀不溶解,则该溶液不可能是( )
| A. | Na2CO3 | B. | AgNO3 | C. | Na2SO3 | D. | Na2SO4 |
6.下列各组物质中化学键类型完全相同的是( )
| A. | HI和NaI | B. | H2S和CO2 | C. | Cl2和CCl4 | D. | F2和NaBr |
13.4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性.(CN)2称为拟卤素,性质与卤素相似.下列说法不正确的是( )
| M | N | ||
| X | Y |
| A. | X位于三周期 IIA,其单质可采用电解熔融MgCl2制备 | |
| B. | 元素最高价氧化物的水化物中,酸性最强的是HNO3 | |
| C. | 气体分子(MN)2 的电子式为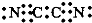 | |
| D. | (MN)2其与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2=2NaCN+H2O |
10.硅是一种重要的非金属单质,其化学性质与碳既有相似之处,也有不同之处.在常温下,下列物质能够与硅发生反应的是( )
| A. | HF | B. | HNO3 | C. | NaCl | D. | H2SO4 |
10.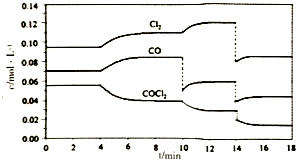 光气的分解反应为:COCl2(g)?Cl2(g)+CO(g)△H>0,反应体系达平衡后,各物质的浓度在不同条件下的变化状况如图所示,则下列说法正确的是( )
光气的分解反应为:COCl2(g)?Cl2(g)+CO(g)△H>0,反应体系达平衡后,各物质的浓度在不同条件下的变化状况如图所示,则下列说法正确的是( )
 光气的分解反应为:COCl2(g)?Cl2(g)+CO(g)△H>0,反应体系达平衡后,各物质的浓度在不同条件下的变化状况如图所示,则下列说法正确的是( )
光气的分解反应为:COCl2(g)?Cl2(g)+CO(g)△H>0,反应体系达平衡后,各物质的浓度在不同条件下的变化状况如图所示,则下列说法正确的是( )| A. | 从第10min到第12min时,生成Cl2的速率v(Cl2)=0.01mol•L-1•min-1 | |
| B. | 第8min时与第18min时反应的平衡常数相同 | |
| C. | 由于10min时条件的改变,使COCl2的转化率降低 | |
| D. | 在第14min时,改变的条件可能是压缩反应容器的体积 |