题目内容
6.下列各组物质中化学键类型完全相同的是( )| A. | HI和NaI | B. | H2S和CO2 | C. | Cl2和CCl4 | D. | F2和NaBr |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,据此分析解答.
解答 解:A.HI分子中H-I原子之间只存在共价键,NaI中钠离子和碘离子之间只存在离子键,所以化学键类型不同,故A错误;
B.硫化氢、二氧化碳分子中都只含共价键,且都是极性键,故B正确;
C.氯气分子中Cl-Cl原子之间只存在非极性键,四氯化碳分子中C-Cl原子之间只存在极性键,故C错误;
D.氟气分子中F-F原子之间只存在非极性键,溴化钠中钠离子和溴离子之间只存在离子键,故D错误;
故选B.
点评 本题考查化学键,侧重考查基本概念,明确物质构成微粒之间作用力即可解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列几组化合物,化学键类型不相同的是( )
| A. | NH3和H2O | B. | Na2O和MgCl2 | C. | H2S和Na2S | D. | NaOH和NH4Cl |
17.现有X、Y、Z、M四种短周期元素,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍.下列说法不正确的是( )
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 简单离子半径由大到小的顺序是:Z>M>Y | |
| C. | 气态氢化物的稳定性:Z<M | |
| D. | 等浓度的X2Z与Y2Z的溶液中,水的电离程度:X2Z<Y2Z |
14.某无色透明的酸性溶液能与铁反应生成氢气,则该溶液中一定能够大量共存的是( )
| A. | NH4+、K+、Ba2+、Cl- | B. | Na+、K+、Cl-、SiO32- | ||
| C. | SO42-、Na+、Cu2+、Cl- | D. | SO42-、NO3-、K+、Na+ |
11.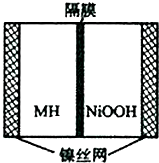 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )
 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )| A. | 放电时负极反应为:MH+OH--e-→M+H2O | |
| B. | 电池的电解液可为KOH溶液,OH-向负极移动 | |
| C. | 放电时正极反应为:NiOOH+H2O-e-→Ni(OH)2+OH- | |
| D. | MH是一类储氢材料,其氢密度越大,电池的能量密度越高 |
18.666℃和1.01×105 Pa时,反应“CaCO3(s)═CaO(s)+CO2(g)△H=+178.3kJ/mol”能自发进行的原因是( )
| A. | 温度升高 | B. | 该反应熵增 | ||
| C. | 熵增效应大于能量效应 | D. | 反应速率加快 |
15.W、R、X、Y、Z是五种短周期元素,部分信息如表所示:
请回答下列问题:
(1)Z的元素符号可能是H、Be、Al;
(2)XW3能使红色湿润石蕊试纸变蓝色;
(3)Y和R元素组成常见的化合物的化学式为CO2或SiO2;
(4)画出Y的简单离子结构示意图: .
.
| 元素代号 | 部分信息 |
| W | W是一种核素没有中子 |
| R | R原子的最外层电子数等于K层电子数的2倍 |
| X | X原子得到3个电子达到稳定结构,单质在常温、常压下呈气态 |
| Y | Y原子的最外层电子数是电子层数的3倍 |
| Z | Z原子的电子层数等于最外层电子数 |
(1)Z的元素符号可能是H、Be、Al;
(2)XW3能使红色湿润石蕊试纸变蓝色;
(3)Y和R元素组成常见的化合物的化学式为CO2或SiO2;
(4)画出Y的简单离子结构示意图:
 .
.
15.化学与生活密切相关,下列说法正确的是( )
| A. | 绿色食品是只指纯天然食品,不含任何化学物质 | |
| B. | 推广使用可降解塑料及布质购物袋,以减少“白色污染” | |
| C. | 为消除碘缺乏病,政府规定在食盐中必须添加一定量的KI | |
| D. | 只要带专用口罩,就不怕雾霾天气对人体产生伤害 |
 下列各组物质,不能按照图关系相互转化的是(“→”表示反应一步完成)( )
下列各组物质,不能按照图关系相互转化的是(“→”表示反应一步完成)( )