题目内容
【题目】右图为原电池示意图,回答下列问题:
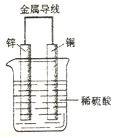
(1)该装置能够将_________能转化成电能。
(2)锌是原电池的_______极,放电过程中____(填“得”或“失”)电子,发生_______反应。
(3)电子是由_______极通过导线流向________极。
(4)铜电极的电极的反应式为____________________
(5)总反应的化学方程式为_______________________
【答案】 化学 负 失 氧化 负 正 2H++2e-=H2↑ Zn+H2SO4=ZnSO4+H2
【解析】(1)该装置是原电池,原电池是将化学能转化为电能的装置;(2)较活泼的金属作为负极,锌是原电池的负极,放电过程中失去电子,发生氧化反应;(3)电子是由负极通过导线流向正极;(4)铜电极作为正极,氢离子在正极得电子产生氢气,电极的反应式为:2H++2e=H2↑;(5)负极锌失去电子产生锌离子,电极反应式为:Zn-2e-=Zn2+,总反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑。

 阅读快车系列答案
阅读快车系列答案【题目】镓与ⅤA族元素形成的化合物是重要的半导体材料,应用最广泛的是砷化镓(GaAs)。回答下列问题:
(1)基态Ga原子的核外电子排布式为__________,基态As原子核外有__________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为__________和+3。砷的电负性比镓__________(填“大”或“小”)。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:__________________________。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是_______________________________________。
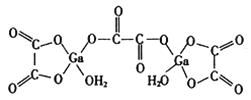
(4)二水合草酸镓的结构如图所示,其中镓原子的配位数为__________,草酸根中碳原子的杂化方式为__________。
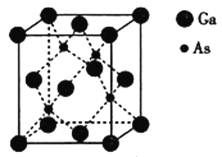
(5)砷化镓熔点为1238℃,立方晶胞结构如图所示,晶胞参数为a=565pm,该晶体的类型为__________,晶体的密度为__________(设NA为阿伏加德罗常数的数值,列出算式即可)g·cm-3。
【题目】几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | R | Q | U | |
原子半径( | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | 0.82 | |
主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | +3 | |
最低负价 | -1 | -3 | -2 | |||||
下列说法错误的是( )
A. 元素X和Q形成的化合物中不可能含有共价键
B. X、Z、R的最高价氧化物的水化物之间可两两相互反应
C. R3-比Q2-更容易失去电子
D. M(OH)2的碱性比XOH的碱性弱
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | 淀粉-KI 溶液 | 氧化性:Cl2>I2 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
【题目】80℃时,2 L密闭容器中充入0.40 mol N2O4,发生如下反应:N2O4(g)![]() 2NO2(g)。一段时间后达到平衡,测得数据如下:
2NO2(g)。一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/( mol·L1) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
请回答:
(1)20 s内,v(NO2) =_________mol/(L·s) 1。
(2)升高温度时,c(NO2)增大,则正反应是______(选填“放热”或“吸热”)反应。
(3)该温度下反应的化学平衡常数数值为______。
(4)该条件下N2O4的平衡转化率是______。