题目内容
【题目】某研究性学习小组的同学用以下仪器组合的装置制取氯气,并探究其性质。
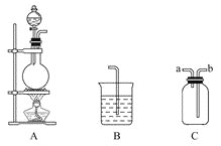
请回答下列问题:
(1)实验室制取氯气的化学方程式为___;检查图中反应器气密性的方法是___。
(2)现要求从图中选用所需的仪器(可重复选用)组成一套制取纯净、干燥氯气的装置,实验时要防止污染。下表是按仪器的连接顺序由上至下依次填写的,请将该表填写完整(加入的试剂自选)。______。
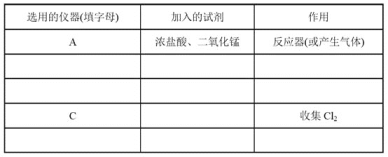
(3)该实验中用仪器C收集Cl2时,进气口应为___(填字母)。
(4)将氯气通入紫色石蕊试液中,可观察到溶液先变红后褪色的现象,出现这种现象的原因是___。
(5)人若吸入大量氯气会中毒死亡。某地化工厂的储氯罐意外发生泄漏,周围被疏散的群众应采取的自救措施是_______。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 关闭分液漏斗的活塞,末端连接导管,将导气管插入水中,用双手捂住烧瓶(或用酒精灯微热烧瓶),若导气管口有气泡冒出,松手后导气管中能形成一段稳定水柱,则说明气密性良好
MnCl2+Cl2↑+2H2O 关闭分液漏斗的活塞,末端连接导管,将导气管插入水中,用双手捂住烧瓶(或用酒精灯微热烧瓶),若导气管口有气泡冒出,松手后导气管中能形成一段稳定水柱,则说明气密性良好  b 氯气与水反应生成盐酸和次氯酸,盐酸能使石蕊试液变红,次氯酸能使石蕊试液褪色 先用水或弱碱性溶液将毛巾润湿后捂住口鼻,然后尽量沿逆风方向向地势较高处跑
b 氯气与水反应生成盐酸和次氯酸,盐酸能使石蕊试液变红,次氯酸能使石蕊试液褪色 先用水或弱碱性溶液将毛巾润湿后捂住口鼻,然后尽量沿逆风方向向地势较高处跑
【解析】
(1)实验室制备Cl2是用MnO2氧化浓盐酸,该装置的气密性检查应用加热法;
(2)由于MnO2与浓盐酸制得的Cl2中含有HCl、H2O,需除去,所以连接顺序为制气→除HCl→干燥→收集→尾气吸收,据此解答;
(3)由于Cl2密度大于空气,应用向上排空气法收集,应为长进短处;
(4) Cl2+H2O![]() HCl+HClO,HCl呈酸性,HClO具有漂白性,据此解答;
HCl+HClO,HCl呈酸性,HClO具有漂白性,据此解答;
(5)Cl2密度大于空气, 且Cl2与碱液反应,据此解答。
(1)实验室制备Cl2是用MnO2氧化浓盐酸,该装置的气密性检查应关闭分液漏斗的活塞,将导气管插入水中,用双手捂住烧瓶(或用酒精灯微热烧瓶),若导气管口有气泡冒出,松手后导气管中能形成一段稳定水柱,则说明气密性良好,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;关闭分液漏斗的活塞,将导气管插入水中,用双手捂住烧瓶(或用酒精灯微热烧瓶),若导气管口有气泡冒出,松手后导气管中能形成一段稳定水柱,则说明气密性良好;
MnCl2+Cl2↑+2H2O;关闭分液漏斗的活塞,将导气管插入水中,用双手捂住烧瓶(或用酒精灯微热烧瓶),若导气管口有气泡冒出,松手后导气管中能形成一段稳定水柱,则说明气密性良好;
(2)由于MnO2与浓盐酸制得的Cl2中含有HCl、H2O,需除去,所以连接顺序为制气→除HCl→干燥→收集→尾气吸收,仪器组合为A→C→C→C→B,对应的试剂和作用为:C;饱和氯化钠溶液;除去HCl;C;浓硫酸;除去H2O;B;NaOH溶液;吸收多余的Cl2;故答案为:C;饱和氯化钠溶液;除去HCl;C;浓硫酸;除去H2O;B;NaOH溶液;吸收多余的Cl2;
(3)由于Cl2密度大于空气,应用向上排空气法收集,则b管进气,a管出气,故答案为:b;
(4) 将氯气通入紫色石蕊试液中,可观察到溶液先变红后褪色的现象,是因为Cl2+H2O![]() HCl+HClO,溶液呈酸性,但是HClO具有强氧化性,能漂白指示剂,故答案为:氯气与水反应生成盐酸和次氯酸,盐酸能使石蕊试液变红,次氯酸能使石蕊试液褪色;
HCl+HClO,溶液呈酸性,但是HClO具有强氧化性,能漂白指示剂,故答案为:氯气与水反应生成盐酸和次氯酸,盐酸能使石蕊试液变红,次氯酸能使石蕊试液褪色;
(5)由于Cl2密度大于空气, Cl2与碱液反应,所以先用水或弱碱性溶液将毛巾润湿后捂住口鼻,然后尽量沿逆风方向向地势较高处跑,故答案为:先用水或弱碱性溶液将毛巾润湿后捂住口鼻,然后尽量沿逆风方向向地势较高处跑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
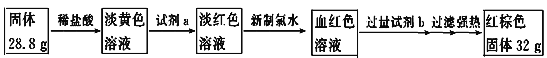
小学生10分钟应用题系列答案【题目】三氯化钌广泛应用于氯碱工业中金属阳极钌涂层及加氢催化剂。现以固体含Ru废料为原料制备RuCl3晶体,其工艺流程如下:
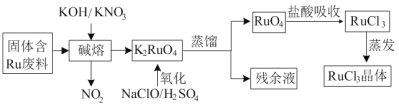
回答下列问题:
(1)K2RuO4中Ru的化合价为_____,“碱熔”中产生的气体可用于____(写一种工业用途)。
(2)“氧化”时欲使2mol K2RuO4氧化为RuO4,则需要氧化剂的物质的量为______mol。
(3)为了提高“碱熔”效率,可以采取的措施有______。
(4)RuO4气体有剧毒,“盐酸吸收”时的化学方程式为___________。
(5)可用氢还原重量法测定产品的纯度,其原理为2RuCl3+3H2 = 2Ru+6HCl,所得实验数据记录如下:
实验序号 | 产品质量/g | 固体Ru质量/g |
① | 5.1875 | 2.0210 |
② | 5.1875 | 2.0190 |
③ | 5.1875 | 2.0200 |
④ | 5.1875 | 1.6200 |
则产品的纯度为________(用百分数表示)。
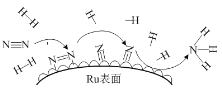
(6)钌及其化合物在合成工业上有广泛用途,根据图示写出合成反应的化学方程式________。