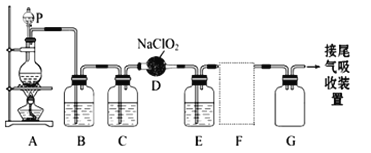
题目内容
【题目】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图的所示的转化关系。由此推断:
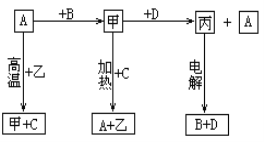
(1)甲的化学式为_____________,丙的化学式为______________。
(2)写出甲和D反应的化学方程式___________________________________________。
(3)为检验化合物甲中元素的化合价,需要用到的药品有_________________________。
A.稀硫酸 B.盐酸 C.硫氰化钾溶液 D.高锰酸钾溶液
(4)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:
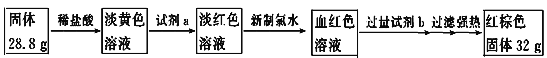
化合物甲的质量分数为________________。
【答案】 Fe3O4 Al2O3 3Fe3O4 +8Al ![]() 9Fe +4Al2O3 A、C、D 80.6%
9Fe +4Al2O3 A、C、D 80.6%
【解析】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价,则A是Fe,乙是H2O,甲是Fe3O4;B是O2,C是H2,D是Al,丙是Al2O3。(1) 甲的化学式为Fe3O4,丙的化学式为Al2O3;(2)甲和D在高温下发生铝热反应,产生Al2O3和Fe,反应的化学方程式是3Fe3O4 +8Al ![]() 9Fe +4Al2O3;(3)化合物甲是Fe3O4,要检验其中所含有的阳离子,要先用非氧化性的酸使其发生反应:Fe3O4+8H+= 2Fe3++Fe2+ +4H2O,然后在用高锰酸钾溶液检验Fe2+;用硫氰化钾溶液检验Fe3+,故使用的物质是A、C、D;(4)Fe与水蒸气反应产生Fe3O4,要测其含量,最后得到的红棕色的固体是Fe2O3,其物质的量是
9Fe +4Al2O3;(3)化合物甲是Fe3O4,要检验其中所含有的阳离子,要先用非氧化性的酸使其发生反应:Fe3O4+8H+= 2Fe3++Fe2+ +4H2O,然后在用高锰酸钾溶液检验Fe2+;用硫氰化钾溶液检验Fe3+,故使用的物质是A、C、D;(4)Fe与水蒸气反应产生Fe3O4,要测其含量,最后得到的红棕色的固体是Fe2O3,其物质的量是![]() ,n(Fe)=0.2mol×2=0.4mol,假设在28.8g中含有Fe、Fe3O4的物质的量分别是x、y,则x+3y=0.4mol,56x+232y=28.8g,解得x=0.1mol,y=0.1mol,所以化合物甲的质量分数为
,n(Fe)=0.2mol×2=0.4mol,假设在28.8g中含有Fe、Fe3O4的物质的量分别是x、y,则x+3y=0.4mol,56x+232y=28.8g,解得x=0.1mol,y=0.1mol,所以化合物甲的质量分数为![]()

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】碘在科研与生活中有重要应用.某兴趣小组用0.50molL﹣1KI、0.2%淀粉溶液、0.20molL﹣1K2S2O8、0.10molL﹣1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.已知: S2O82﹣+2I﹣═2SO42﹣+I2(慢) I2+2S2O32﹣═2I﹣+S4O62﹣(快)
(1)向KI,Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的耗尽后,溶液颜色将由无色变成为蓝色.其中该反应速率快慢的是由(填“第一个”或“第二个”)反应决定的.为确保能观察到蓝色,S2O32﹣与S2O82﹣初始的物质的量需满足的关系为:n(S2O32﹣):n(S2O82﹣) .
(2)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积/mL溶液 | ||||
K2S2O8溶液 | H2O | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | V1 | V3 | 4.0 | 2.0 |
③ | 8.0 | V2 | V4 | V5 | 2.0 |
表中V3、V4和V5取实验设计的体积数值,目的是 , 表中的V2= , 理由是 .