题目内容
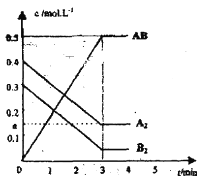
【题目】在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)![]() A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A.平均反应速度:甲<乙B.平衡时C的物质的量:甲>乙
C.平衡时C的转化率:甲>乙D.平衡时混合气体密度:甲<乙
【答案】B
【解析】
A、由于甲中压强大于乙中压强,因此反应速率:甲>乙,选项A错误;
B、甲为恒容,乙为恒压,随着反应的进行,甲中压强大于乙中压强,乙容器中反应更容易向正反应方向进行,平衡时C的物质的量:甲>乙,选项B正确;
C、甲为恒容,乙为恒压,随着反应的进行,甲中压强大于乙中压强,乙容器中反应更容易向正反应方向进行,因此C的转化率乙>甲,选项C错误;
D、甲为恒容,乙为恒压,随着反应的进行,甲中压强大于乙中压强,甲中体积小于乙中体积,气体总质量不变,则密度:甲>乙,选项D错误;
答案选B。

 阅读快车系列答案
阅读快车系列答案【题目】为测定![]() 样品的纯度,用硫酸溶解6.300 g样品,定容至250 mL。取25.00 mL溶液,用
样品的纯度,用硫酸溶解6.300 g样品,定容至250 mL。取25.00 mL溶液,用![]() 标准溶液滴定至终点。重复实验,数据如下:
标准溶液滴定至终点。重复实验,数据如下:
序号 | 滴定前读数/mL | 滴定终点读数/mL |
1 | 0.00 | 19.98 |
2 | 1.26 | 22.40 |
3 | 1.54 | 21.56 |
已知:![]()
假设杂质不参加反应。
该样品中![]() 的质量分数是________%(保留小数点后一位);
的质量分数是________%(保留小数点后一位);
写出简要计算过程:________。
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺流程如下:

已知: ① 硫酸浸取液中的金属离子主要是Cr3+,其次是Fe2+、Al3+、Ca2+和Mg2+。
② Cr2O72-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
③ 常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
沉淀完全时的pH | 3.2 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1)实验室用18.4mol/L的浓硫酸配制500mL2mol/L的硫酸时除用量筒、烧杯和玻璃棒外,还需用到的玻璃仪器有_________________________。
(2)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式__________。
(3)过滤II操作得到的滤渣主要为______(填化学式)。
(4)钠离子交换树脂的反应原理为:Mn++nNaR=MRn+nNa+,则利用钠离子交换树脂可除去滤液II中的金属阳离子有_________________。
(5)上述流程中,每还原1molCrO42-时,需要消耗SO2 _______ mol。