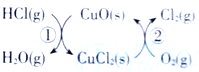��Ŀ����
����Ŀ������M��һ���ճ������в���ȱ�ٵĵ�ζƷ����֪C����D��ȼ�շ�����ɫ���档M���������ʵ�ת����ϵ����ͼ��ʾ(���ֲ�������ȥ)��

��1��д���ö��Ե缫���M��Һ�����ӷ���ʽ_______________________��
��2����A��һ������������ҿ��������첣������G�Ļ�ѧʽ��_________________��
��3����A��һ�ֳ����������ʣ���A��B��Һ�ܹ���Ӧ��������F��Һ��μ���E��Һ���ӱ�����������ʵ��������_______________��
��4����A��һ���Σ�A��Һ��B��Һ��ϲ�����ɫ��״������˲���Ϊ����ɫ������ɺ��ɫ��E������Aת����E�����ӷ���ʽ��__________________________________��
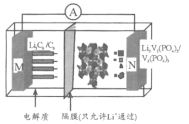
��5����A��һ����Һ��ֻ���ܺ���![]() �е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ��ʾ���ɴ˿�֪������Һ�п϶����е����Ӽ���Ũ��֮��Ϊ_________��
�е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ��ʾ���ɴ˿�֪������Һ�п϶����е����Ӽ���Ũ��֮��Ϊ_________��

���𰸡�2Cl+2H2O![]() 2OH+H2��+Cl2�� H2SiO3 ��Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ 4Fe2++8OH+O2+2H2O = 4Fe(OH)3�� c(H+)��c(Al3+)��c(NH4+)��c(SO42)=1:1:2:3
2OH+H2��+Cl2�� H2SiO3 ��Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ 4Fe2++8OH+O2+2H2O = 4Fe(OH)3�� c(H+)��c(Al3+)��c(NH4+)��c(SO42)=1:1:2:3
��������
C����D��ȼ�շ�����ɫ���棬��֪���߷ֱ�ΪH2��Cl2��FΪHCl������M��һ���ճ������в���ȱ�ٵĵ�ζƷ��ΪNaCl����BΪNaOH ��
��1���ö��Ե缫���NaCl��Һ������NaOH��H2��Cl2�����ӷ���ʽΪ��2Cl+2H2O![]() 2OH+H2��+Cl2����
2OH+H2��+Cl2����
��2����A��һ������������ҿ��������첣������AΪSiO2����NaOH��Ӧ���ɵ�EΪNa2SiO3����HCl��Ӧ���ɵ�GΪH2SiO3��
��3��A��һ�ֳ����������ʣ�����NaOH��Һ��Ӧ����AΪAl��EΪNa[Al(OH)4]����������������μ���Na[Al(OH)4]��Һ���ӱ���Na[Al(OH)4]����HCl��Ӧ����Al(OH)3����������HCl��Al(OH)3��HCl��Ӧ����AlCl3������ʵ������Ϊ����Һ�����а�ɫ��״�������ɣ��Ҳ������ӣ�Ȼ�����ɶൽ�٣������ʧ��
��4��A��Һ��B��Һ��ϲ�����ɫ��״������˲���Ϊ����ɫ������ɺ��ɫ��E����A�к�Fe2+�����ɵ�EΪFe(OH)3�������ķ�Ӧ�У�Fe2++2OH=Fe(OH)2����4Fe(OH)2+O2+2H2O=4Fe(OH)3��������Ӧ�ӺͿɵ����ӷ���ʽ��4Fe2++8OH+O2+2H2O = 4Fe(OH)3����
��5������ͼ����ͼ���м��뵥λ�����NaOH��Һ��NaOHΪ1mol�������һ����NaOHû�г������ɣ������ķ�ӦΪ��OH+H+=H2O����ԭ��Һ��H+�����ʵ���Ϊ1mol����������3mol NaOH���ɳ�����������1mol NaOH��Al(OH)3�ܽ⣬��ԭ��Һ��Al3+�����ʵ���Ϊ1mol����Mg2+��Fe3+��CO32һ�������ڣ��м����2mol NaOH���������䣬�����ķ�ӦΪOH��NH4+��Ӧ����ԭ��Һ��NH4+�����ʵ���Ϊ2mol��������ֻ��ΪSO42�����ݵ���غ�ɵ�SO42�����ʵ���Ϊ3mol������c(H+)��c(Al3+)��c(NH4+)��c(SO42)=1:1:2:3��

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�����Ŀ����ͼ��Ԫ�����ڱ��Ŀ�ܣ����ڱ��Т١���Ԫ���лش����⡣
�� |
|
| |||||||||||||||
|
|
|
|
| �� | �� | �� |
| |||||||||
�� | �� | �� |
|
|
| �� |
| ||||||||||
�� |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| �� |
|
��ش��������⣺
��1��Ԫ�آڵ�ԭ�ӽṹʾ��ͼ��___��
��2���ڱ��Тܡ��ݡ�������Ԫ�صļ����Ӱ뾶��С�����˳��Ϊ___�������ӷ��ţ���
��3�����Тݵ�����������ˮ������ߵ���������ﷴӦ�����ӷ���ʽΪ____��
��4�����������Ԫ�طǽ�����ǿ����___����Ԫ�ط��ţ���