题目内容
【题目】白色固体PCl5受热即挥发并发生分解:PCl5(g)![]() PCl3(g)+Cl2(g)。现将5.84 g PCl5装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105Pa,经计算可知平衡时容器内混合气体的物质的量为0.05 mol,求平衡时PCl5的分解率__________。
PCl3(g)+Cl2(g)。现将5.84 g PCl5装入2.05 L真空密闭容器中,在277 ℃达到平衡,容器内压强为1.01×105Pa,经计算可知平衡时容器内混合气体的物质的量为0.05 mol,求平衡时PCl5的分解率__________。
【答案】78.6%
【解析】
计算PCl5的起始物质的量,利用差量法计算参加反应的PCl5的物质的量,进而计算平衡时PCl5的分解率。
5.84gPCl5的物质的量为![]() =0.028mol,设参加反应PCl5的物质的量为x,则:
=0.028mol,设参加反应PCl5的物质的量为x,则:
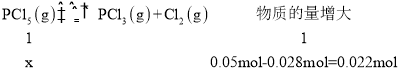
故x=0.022mol,则平衡时PCl5的分解率![]() ,故答案为:平衡时PCl5的分解率为78.6%。
,故答案为:平衡时PCl5的分解率为78.6%。

练习册系列答案
相关题目
【题目】如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
① |
|
| |||||||||||||||
|
|
|
|
| ② | ③ | ④ |
| |||||||||
⑤ | ⑥ | ⑦ |
|
|
| ⑧ |
| ||||||||||
⑨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ⑩ |
|
请回答下列问题:
(1)元素②的原子结构示意图是___。
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为___(填离子符号)。
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为____。
(4)⑧与⑩两种元素非金属较强的是___(填元素符号)。