题目内容
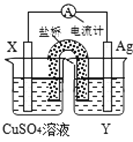
【题目】在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示。
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示。

(1)在上述反应达到平衡后,第4min时,若将容器的体积快速扩大一倍(其他条件不变),请在图中画出4min~5min的AB浓度的变化线。____
(2)在相同条件下,若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol。则反应开始时v正____v逆 (填“>”、“<”或“=”)。判断依据是____________________________________________________。反应达到平衡后,各物质的体积分数与原平衡相比____(填序号)
①A2、B2减小,AB增大 ②A2、B2增大,AB减小 ③均不变 ④无法确定
【答案】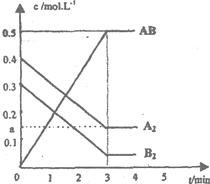 > 因为此时 所以平衡向正反应方向移动,v正>v逆 ③
> 因为此时 所以平衡向正反应方向移动,v正>v逆 ③
【解析】
(1)上述反应达到平衡后,第4min时,若把容器的体积快速扩大一倍,瞬间AB的浓度变为原来的一半,该反应反应前后气体体积不变,压强只改变反应速率,不改变平衡移动;
(2)根据图可知,平衡时AB的浓度变化为0.5mol/L,则A2的浓度变化为0.25mol/L,所以a=0.4mol/L-0.25mol/L=0.15mol/L,平衡时B2的浓度为0.3mol/L-0.25mol/L=0.05mol/L,根据K=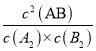 计算平衡常数,计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行;
计算平衡常数,计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行;
若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol,等效为开始加入加入0.8mol的A2气体和0.6molB2气体,与原平衡为完全等效平衡,平衡时相同组分的物质的量浓度相等。
(1)上述反应达到平衡后,第4min时,若把容器的体积快速扩大一倍,瞬间AB的浓度变为原来的一半,该反应反应前后气体体积不变,压强只改变反应速率,不改变平衡移动,4min~5min的AB浓度的变化线为: ;
;
(2)根据图可知,平衡时AB的浓度变化为0.5mol/L,则A2的浓度变化为0.25mol/L,所以a=0.4mol/L-0.25mol/L=0.15mol/L,平衡时B2的浓度为0.3mol/L-0.25mol/L=0.05mol/L,平衡常数K=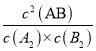 =
=![]() =
=![]() ,
,
若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol,浓度商Qc=![]() =8<K=
=8<K=![]() ,反应向正反应进行,
,反应向正反应进行,
若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol,等效为开始加入加入0.8mol的A2气体和0.6molB2气体,恒温恒容下,与原平衡为完全等效平衡,平衡时相同组分的物质的量浓度相等,反应达到平衡后,各物质的体积分数与原平衡相比均不变。

【题目】如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
① |
|
| |||||||||||||||
|
|
|
|
| ② | ③ | ④ |
| |||||||||
⑤ | ⑥ | ⑦ |
|
|
| ⑧ |
| ||||||||||
⑨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ⑩ |
|
请回答下列问题:
(1)元素②的原子结构示意图是___。
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为___(填离子符号)。
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为____。
(4)⑧与⑩两种元素非金属较强的是___(填元素符号)。