题目内容
20.下列反应的离子方程式正确( )| A. | 铜与稀硝酸反应 Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O | |
| B. | 稀碳酸钠溶液中通入二氧化碳 CO32-+CO2+H2O=2HCO3- | |
| C. | 在氯化铝溶液中滴入氨水 Al3++4NH3•H2O=AlO2-+4NH4+ | |
| D. | 向次氯酸钙溶液中通入SO2 Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
分析 A.铜与稀硝酸反应生成一氧化氮气体,不是生成二氧化氮;
B.碳酸钠溶液与二氧化碳反应生成碳酸氢钠;
C.氨水为弱碱,二者反应生成氢氧化铝沉淀;
D.次氯酸具有强氧化性,能够氧化亚硫酸钙,反应生成的是硫酸钙沉淀.
解答 解:A.铜与稀硝酸反应生成硝酸铜、NO气体和水,正确的离子方程式为:3Cu+2NO3-+8H+=2Cu2++2NO↑+4H2O,故A错误;
B.稀碳酸钠溶液中通入二氧化碳,反应生成碳酸氢钠,反应的离子方程式为:CO32-+CO2+H2O=2HCO3-,故B正确;
C.在氯化铝溶液中滴入氨水,反应生成氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.向次氯酸钙溶液中通入SO2,亚硫酸钙被氧化成硫酸钙,正确的离子方程式为:Ca2++3ClO-+H2O+SO2═CaSO4↓+2HClO+Cl-,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列排列顺序正确的是( )
| A. | 原子序数:C>Li>B | B. | 元素的非金属性:N>O>F | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 氢化物的稳定性:HF>HCl>HBr |
8.下列排序不正确的是( )
| A. | 稳定性 PH3<H2S<HCl | B. | 沸点高低 NH3<PH3<AsH3 | ||
| C. | 还原性 Br-<Fe2+<I- | D. | 微粒半径 K+<Cl?<S2? |
15.一定温度下,在一固定体积的密闭容器中,可逆反应A(s)+3B(g)?2C(g)达到平衡时,下列说法正确的是( )
①C的生成速率和C的分解速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化 ④混合气体的总压强不再变化 ⑤A、B、C物质的量之比为1:3:2
⑥混合气体的平均相对分子质量不变 ⑦容器中C的体积分数不变.
①C的生成速率和C的分解速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③气体密度不再变化 ④混合气体的总压强不再变化 ⑤A、B、C物质的量之比为1:3:2
⑥混合气体的平均相对分子质量不变 ⑦容器中C的体积分数不变.
| A. | ②④⑤⑦ | B. | ①③④⑥⑦ | C. | ①④⑥⑦ | D. | ①③④⑤ |
5.对于实验Ⅰ~Ⅳ的实验现象预测正确的是(
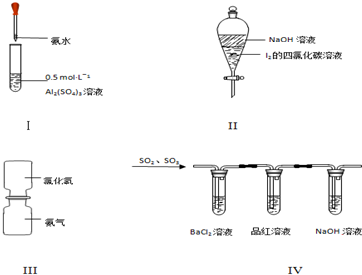

| A. | 实验Ⅰ:试管中先出现白色胶状物质,后溶解 | |
| B. | 实验Ⅱ:振荡后静置,下层溶液颜色保持不变 | |
| C. | 实验Ⅲ:抽去中间玻璃片,瓶内没有任何现象 | |
| D. | 实验Ⅳ:BaCl2溶液变浑浊,品红溶液褪色 |
12.能量之间是可以相互转化的.下列过程中,有电能转化为化学能的是( )
| A. | 电解水 | B. | 光合作用 | C. | 打手机 | D. | 点燃氢气 |
10.往100mL氢离子浓度为1mol•L-1的硫酸和硝酸混合液中投入3.84g铜粉,微热使反应充分完成后,生成NO气体448mL(标准状况).则反应前的混合液中含硫酸的物质的量为( )
| A. | 0.01mol | B. | 0.02 mol | C. | 0.03 mol | D. | 0.04 mol |
 .
.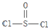 )是一种很重要的化学试剂,可以作为氯化剂和脱水剂.氯化亚砜分子的几何构型是三角锥形;中心原子采取SP3杂化方式.
)是一种很重要的化学试剂,可以作为氯化剂和脱水剂.氯化亚砜分子的几何构型是三角锥形;中心原子采取SP3杂化方式.