题目内容
设NA为阿伏加德罗常数的值,下列叙述错误的是( )
| A、18g H2O中含有的质子数为10NA |
| B、1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| C、46g NO2和N2O4混合气体中含有原子总数为3NA |
| D、常温常压下,22.4L N2和O2的混合气体中含有的分子数目为NA |
考点:阿伏加德罗常数
专题:离子反应专题
分析:A.水分子中含有10个电子,18g水的物质的量为:
=1mol,1mol水中含有10mol质子;
B.钠为1价金属,1mol钠完全反应,无论生成氧化钠还是过氧化钠,都失去1mol电子;
C.NO2和N2O4的最简式为NO2,根据二者的最简式计算出混合物中含有原子总数;
D.常温下,气体摩尔体积大于22.4L/mol,22.4L氮气和氧气的混合气体的物质的量小于1mol.
| 18g |
| 18g/mol |
B.钠为1价金属,1mol钠完全反应,无论生成氧化钠还是过氧化钠,都失去1mol电子;
C.NO2和N2O4的最简式为NO2,根据二者的最简式计算出混合物中含有原子总数;
D.常温下,气体摩尔体积大于22.4L/mol,22.4L氮气和氧气的混合气体的物质的量小于1mol.
解答:
解:A.18g水的物质的量为:
=1mol,含有10mol质子,含有的质子数为10NA,故A正确;
B.1mol Na与足量O2反应,无论生成Na2O还是Na2O2,根据电子守恒,1mol钠失去1mol电子,失去NA个电子,故B正确;
C.46gNO2和N2O4的含有NO2的物质的量为:
=1mol,含有原子的总物质的量为3mol,含有原子总数为3NA,故C正确;
D.常温常压下,气体摩尔体积大于22.4L/mol,22.4L N2和O2的混合气体小于1mol,混合气体中含有的分子数目小于NA,故D错误;
故选D.
| 18g |
| 18g/mol |
B.1mol Na与足量O2反应,无论生成Na2O还是Na2O2,根据电子守恒,1mol钠失去1mol电子,失去NA个电子,故B正确;
C.46gNO2和N2O4的含有NO2的物质的量为:
| 46g |
| 46g/mol |
D.常温常压下,气体摩尔体积大于22.4L/mol,22.4L N2和O2的混合气体小于1mol,混合气体中含有的分子数目小于NA,故D错误;
故选D.
点评:本题考查阿伏加德罗常数的有关计算及判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.试题有利于培养学生的逻辑推理能力及灵活运用基础知识解决实际问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用下列实验装置进行相应实验,能达到实验目的是( )
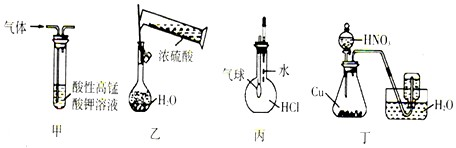

| A、装置甲:除去乙烯中混有的少量SO2 |
| B、装置乙:用浓硫酸配制1mol/L的硫酸 |
| C、装置丙:检验HCl气体在水中的溶解性 |
| D、装置丁:用铜和浓硝酸反应制取NO2 |
下列事实与电化学腐蚀无关的是( )
| A、生铁比纯铁易生锈 |
| B、黄铜(铜锌合金)制品不易产生铜绿 |
| C、纯银饰品久置表面变暗 |
| D、与铜管连接的铁管易生锈 |
“化学无处不在”,下列与化学有关的说法正确的是( )
| A、聚乙烯塑料的老化是因为发生了加成反应 |
| B、纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
| C、合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
| D、向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现紫蓝色,则该溶液含有氨基酸 |
用下列实验装置进行相应实验,不能达到实验目的是( )
A、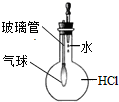 验证HCl极易溶于水 |
B、 石油分馏 |
C、 电解精炼铜 |
D、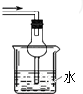 吸收氨气 |
根据下列物质的化学性质,判断其应用错误的是( )
| A、高纯度的硅单质广泛用于制作光导纤维 |
| B、CaO能与SO2反应,可作工业废气的脱硫剂 |
| C、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| D、酒精能使蛋白质变性,可用于杀菌消毒 |
 与Br2发生1:1加成反应,其可能的加成产物的结构简式有:
与Br2发生1:1加成反应,其可能的加成产物的结构简式有: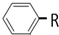 可以被KMnO4酸性溶液氧化成
可以被KMnO4酸性溶液氧化成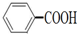 ,但若烷基R中直接与苯环相连的碳原子上没有C-H键,则不易被氧化得到
,但若烷基R中直接与苯环相连的碳原子上没有C-H键,则不易被氧化得到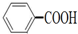 .现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成
.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成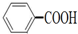 的异构体共有7种,其中两种是
的异构体共有7种,其中两种是 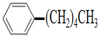 、
、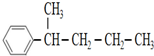 .请写出其他5种的结构简式:
.请写出其他5种的结构简式: