题目内容
7.用C、H、O三种元素组成的物质填空(填化学式):(1)最简单的有机物是CH4;
(2)人类维持生命不可缺少的气体是O2;
(3)既有可燃性,又有还原性的氧化物是CO;
(4)能溶于水,水溶液使紫色石蕊试液变红的气体是CO2.
分析 (1)有机物是指含有碳元素的化合物,最简单的有机物是甲烷;
(2)氧气能够供给呼吸;
(3)三种组成的氧化物有水、双氧水、一氧化碳、二氧化碳,一氧化碳既能燃烧,又具有还原性;
(4)二氧化碳为酸性氧化物,溶于水与水反应生成碳酸,具有酸性,能够使紫色石蕊变红色.
解答 解:(1)最简单的有机物是甲烷,其化学式为:CH4;
故答案为:CH4;
(2)人类维持生命不可缺少的气体是氧气,化学式为:O2;
故答案为:O2;
(3)既有可燃性,又有还原性的氧化物是一氧化碳,化学式:CO;
故答案为:CO;
(4)二氧化碳为酸性氧化物,溶于水与水反应生成碳酸,具有酸性,能够使紫色石蕊变红色,化学式为:CO2;
故答案为:CO2.
点评 本题主要考查物质的性质和用途,解题时注意题干要求,准确书写物质的化学式,题目难度不大.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
17.已知可逆反应aA+bB?cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )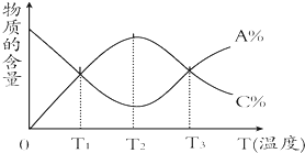

| A. | 该反应在T1、T3温度时达到化学平衡 | |
| B. | 该反应在T2温度时未达到化学平衡 | |
| C. | 升高温度,平衡会向正反应方向移动 | |
| D. | 该反应的正反应是放热反应 |
15.在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)?PCl5(g);5min末达到平衡,有关数据如表.
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 若升高温度,反应的平衡常数减小,则正反应为吸热反应 | |
| B. | 反应5 min内,v(PCl3)=0.08 mol•L-1•min-1 | |
| C. | 当容器中为1.2 mol Cl2时,可逆反应达到平衡状态 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
12.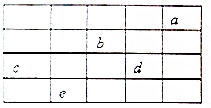 如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )
如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )
 如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )
如图所示,a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是( )| A. | b元素除0价外,只有一种化合价 | |
| B. | 五种元素中,c元素的天然氧化物可被称为刚玉 | |
| C. | b、d气态氢化物溶于水,溶液的酸性:b>d | |
| D. | c、d气态氢化物的稳定性:d>c |
6.取两个相同容积的密闭恒容容器,在A容器中充入0.2molN2O4,B容器中充入0.2molHI气体,在一定温度下反应分别达到平衡,测得N2O4和HI的分解率分别为a(A)和a(B).在该平衡体系中再分别充入0.2molN2O4和0.2molHI,当反应重新达到平衡时,测得N2O4和HI的分解率分别为a′(A)和a′(B).下列判断一定正确的是( )
| A. | a(A)>a′(A) a(B)<a′(B) | B. | a(A)>a′(A) a(B)=a′(B) | C. | a(A)<a′(A) a(B)<a′(B) | D. | a(A)=a′(A) a(B)>a′(B) |
3.在一定条件下,反应A2(g)+B2(g)═2AB(g) 达到平衡状态的是( )
| A. | 单位时间内生成n mol的AB的同时,生成n mol的A2 | |
| B. | 单位时间内生成n mol A2的同时,生成n mol的B2 | |
| C. | 容器内的总压强不随时间而变化 | |
| D. | 单位时间内生成2n mol AB的同时,生成n mol的B2 |
4.下列有关实验的操作、原理和现象,正确的是( )
| A. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)4]溶液,观察铁钉周围出现蓝色沉淀的快慢 | |
| B. | 受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 | |
| C. | 实验室用已知浓度的酯酸溶液滴定未知浓度的氢氧化钠溶液时,选用酚酞做指示剂比用甲基橙做指示剂时带来的误差要大一点 | |
| D. | 自来水厂常用某些含铝或铁的化合物作净水剂,是由于它们具有杀菌作用 |
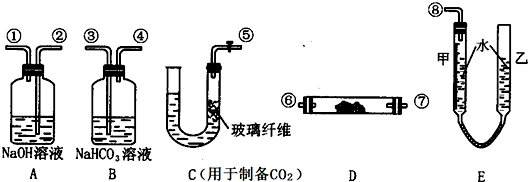
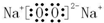 .
.